최소 단어 이상 선택하여야 합니다.
최대 10 단어까지만 선택 가능합니다.
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
NTIS 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
DataON 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Edison 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Kafe 바로가기
| 주관연구기관 | 건국대학교 KonKuk University |
|---|---|
| 연구책임자 | 오덕근 |
| 참여연구자 | 김경록 , 이선화 , 안정웅 , 강우리 , 김민지 , 박지영 , 한정은 , 정연주 |
| 보고서유형 | 최종보고서 |
| 발행국가 | 대한민국 |
| 발행년월 | 2015-10 |
| 주관부처 | 농림축산식품부 |
| 사업 관리 기관 | 농림수산식품기술기획평가원 |
| 등록번호 | TRKO201600000153 |
| DB 구축일자 | 2016-04-02 |
IV. 연구개발결과
가. Hydroxy 지방산 생산
1. Hydratase에 의한 hydroxy 지방산 생산
(1) Lysinibacillus fusiformis 유래 재조합 지방산 hydratase의 반응조건을 최적화하여 40g/L oleic acid와 같은 농도가 함유된 가수분해 올리브유로부터 각각 3시간 및 6시간에 40 g/L 10-hydroxystearic acid를 생산함.
(2) Stenotrophomonas maltophilia 유래 지방산 hydratase 재조합 균주 전세포 개발 및 생산최적화
IV. 연구개발결과
가. Hydroxy 지방산 생산
1. Hydratase에 의한 hydroxy 지방산 생산
(1) Lysinibacillus fusiformis 유래 재조합 지방산 hydratase의 반응조건을 최적화하여 40g/L oleic acid와 같은 농도가 함유된 가수분해 올리브유로부터 각각 3시간 및 6시간에 40 g/L 10-hydroxystearic acid를 생산함.
(2) Stenotrophomonas maltophilia 유래 지방산 hydratase 재조합 균주 전세포 개발 및 생산최적화: 전세포 반응조건을 최적화하여 50 g/L oleic acid를 기질로 하여 4시간 동안 발효 시 49 g/L 10-hydroxystearic acid를 생산함.
(3) 지방산 hydratase 함유 wild-type Stenotrophomonas nitritireducens 전세포 촉매 개발 및 생산 최적화: 전세포 반응조건을 최적화하여 20 g/L linoleic acid를 기질로 하여 3시간동안 반응시 15 g/L 10-hydroxy-12Z-octadecenoic acid 생산함.
(4) L. fusiformis oleate hydratase의 반응조건을 최적화하여 반응 3시간 후에 13.5 g/L10,12-dihydroxystearic acid를 생산함.
(5) 지방산 hydratase 함유 wild-type S. nitritireducens 전세포에 의한 α-linolenic acid에서 10-hydroxy-12,15(Z,Z)- octadecadienoic acid 생산: permeabilized cell을 사용하여 2시간동안 22.5 g/L α-linolenic acid에서 16.4 g/L 10-hydroxy-12,15(Z,Z)- octadecadienoic acid 를 생산함.
(6) Lactobacillus acidophilus linoleate 13-hydratase의 반응조건을 최적화하여 100 g/L linoleic acid로부터 3시간 동안 79 g/L 13-hydroxy-9Z-octadecenoic acid을 생산함.
(7) L. acidophilus linoleate 13-hydratase의 반응조건을 최적화하여 15 g/L α-linolenic acid 로부터 6시간 동안 7.5 g/L 13-hydroxy-12,15 (Z,Z)-octadecadienoic acid를 생산함.
2. Diol synthase에 의한 hydroxy 지방산 생산
(1) Aspergillus nidulans유래 diol synthase 함유 재조합 전세포에 의한 linoleic acid에서 5,8-dihydroxy-9,12(Z,Z)-octadecadienoic acid 생산: 재조합 전세포 23 g/L를 사용하여 5.0 g/L linoleic acid에서 150분 반응하여 5.0 g/L의 5,8-dihydroxy-9,12(Z,Z)-octadecadienoic acid를 얻었음.
(2) A. nidulans유래 diol synthase 함유 재조합 전세포에 의한 α-linolenic acid에서 5,8-dihydroxy-9,12,15(Z,Z,Z)-octadecatrienoic acid 생산: 재조합 전세포 40 g/L를 사용하여 12 g/L α-linolenic acid에서 100분 반응하여 9.1 g/L의 5,8-dihydroxy-9,12,15(Z,Z,Z)-octadecatrienoic acid를 얻었음.
(3) A. nidulans유래 diol synthase 함유 재조합 전세포에 의한 oleic acid에서 5,8-dihydroxy-9(Z)-octadecanoic acid 생산: 재조합 전세포 35 g/L를 사용하여 12 g/L oleic acid에서 60분 반응하여 5.2 g/L의 5,8-dihydroxy-9(Z)-octadecanoic acid를 얻었음.
(4) A. nidulans유래 diol synthase의 peroxygenase 부분만을 활용한 선택적 8R-hydroperoxy-9,12(Z,Z)-octadecadienoic acid 생산: Diol synthase의 variant 함유 재조합 전세포 20 g/L를 사용하여 이용 6 g/L linoleic acid로부터 1시간 반응하여 1.8 g/L 8R-hydroperoxy-9,12(Z,Z)-octadecadienoic acid를 생산함.
(5) Glomerella cingulate유래 diol synthase 함유 재조합 전세포에 의한 linoleic acid에서 7,8-dihydroxy-9,12(Z,Z)-octadecadienoic acid 생산: 재조합 전세포 46 g/L를 사용하여 14g/L linoleic acid에서 120분 반응하여 6.4 g/L의 7,8-dihydroxy-9,12(Z,Z)-octadecadienoic acid를 얻었음.
(6) G. cingulate유래 diol synthase 함유 재조합 전세포에 의한 α-linolenic acid에서 7,8-dihydroxy-9,12,15(Z,Z,Z)-octadecatrienoic acid 생산: 재조합 전세포 46 g/L를 사용하여 14 g/L α-linolenic acid에서 180분 반응하여 6.3 g/L의 7,8-dihydroxy-9,12,15(Z,Z,Z)-octadecatrienoic acid를 얻었음.
(7) G. cingulate유래 diol synthase 함유 재조합 전세포에 의한 oleic acid에서 7,8-dihydroxy-9(Z)-octadecanoic acid 생산: 재조합 전세포 46 g/L를 사용하여 14 g/L oleic acid에서 150분 반응하여 6.4 g/L의 7,8-dihydroxy-9(Z)-octadecanoic acid를 얻었음.
3. Lipoxygenase에 의한 hydroxy 지방산 생산
(1) Nostoc sp. stereo-selective lipoxygenase 의한 linoleic acid에서 9R-hydroxy-10E,12Z-octadecadienoic acid 생산: 재조합 lipoxygenase 함유 전세포반응으로 40 g/L linoleic acid로부터 1시간 반응하여 37.6 g/L 9R-hydroxy-10E,12Z-octadecadienoic acid 확보.
(2) Nostoc sp. 로부터 stereo-selective lipoxygenase 의한 α-linolenic acid에서 9R-hydroperoxy-10E,12Z,15Z-octadecatrienoic acid 생산: 재조합 lipoxygenase 함유 전세포반응으로 40 g/L α-linolenic acid로부터 1시간 반응하여 38.4 g/L 9R-hydroxy-10,12,15(E,Z,Z)-octadecatrienoic acid 확보.
(3) Burkholderia thailandensis lipoxygenase에 의한 linoleic acid에서 13-hydroxy-9,11(Z,E)-octadecadienoic acid 생산: 효소 2.5 g/L를 사용하여 20 g/L linoleic acid에서 1.5시간 반응하여 21 g/L의 13-hydroxy-9,11(Z,E)-octadecadienoic acid를 얻었음.
나. 락톤 생산
1. 막 투과성을 증가시킨 효모 Waltomyces lipofer를 이용하여 10-hydroxystearic acid로부터 γ-dodecalactone의 생산: 효모의 반응조건을 최적화하고 막투과성을 증가시켜 30 g/L 균체를 사용하여 60 g/L 10-hydroxystearic acid로부터 30시간 후에 45.7 g/L γ-dodecalactone를 생산하여 세계 최고의 농도와 생산성 기록함.
2. 지방산을 이용한 효모 W. lipofer의 베타-산화 유도에 의한 hydroxy 지방산으로부터 γ-락톤류의 생산: oleic acid로 베타-산화 유도시켜 10-hydroxystearic acid로부터 γ-dodecalactone의 전환율은 22%, 생산성은 1.3배 향상시킴. 30시간동안 60 g/L의 12-hydroxystearic acid를 기질로 사용하였을 때, 28 g/L의 γ-decalactone을 생산하였고 30시간동안 60 g/L의 10-hydroxydecanoic acid를 기질로 사용하였을 때에는 12 g/L의 γ-butyrolactone을 생산하였음. γ-decalactone의 경우 현재까지 보고된 것보다 2.2배 높은 생산량을 보였으며, 전환율은 13%, 생산성은 5.2배 높은 것으로 나타났고, γ-butyrolactone의 경우에는 생물전환법에 의한 첫 보고임.
3. 10-Hydroxy-12(Z)-octadecenoic acid로부터 γ-dodecelactone 생산: 효모 Candida boidinii의 베타-산화 유도에 의해 5 g/L 10-hydroxy-12(Z)-octadecenoic acid로부터 6시간 반응하여2.2 g/L의 γ-dodecelactone을 생산 (몰수율 64%)하였고 생산성은 350 mg L-1h-1로 나타남.
4. 효모 Yarrowilia lipolytica를 이용하여 13-hydroxy-9-octadecenoic acid로부터 δ-decalactone의 생산: 효모의 반응조건을 최적화하여 세계 최초로 7.5 g/L 13-hydroxy-9-octadecenoic acid로부터 24시간 반응하여 1 g/Lδ-decalactone을 생산
5. 효모 Candida palmiolephila를 이용하여 8-hydroxy-9-octadecenoic acid로부터 Japanese beetle의 pheromone으로 잘 알려진 락톤 japonilure 전환을 확인함.
다. 농산유지로부터 락톤 생산공정 확립
1. Candida rugosa lipase (CRL) lipase에 의한 농산유지 가수분해
5L scale에서 1차년에 선발된 CRL lipase 효소와 가수분해 조건으로 올리브유 가수분하여 oleic acid 함량이 80% 이상 되는 crude oleic acid를 얻을 수 있음.
2. Oleic acid로부터 oleate hydratase 처리에 의한 10-hydroxy stearic acid 생산
시중에서 구매한 oleic acid와 위에서 농산 유지인 올리브유를 가수분해여 얻은 crude oleic acid를 기질로 사용하여 10-hydroxy stearic acid 전환 실험을 수행하고, 얻어진 물질은 NMR로 10-hydroxy stearic acid임을 확인하고, GC 분석 결과 전환율 모두 78% 정도이고 기질의 순도에 따른 전환율에는 차이는 크게 없는 것을 확인함.
3. β-Oxidation (Waltomyces lipofer KCTC 17657) 의한 γ-dodecalactone 생산
위에서 얻은 10-hydroxy stearic acid는 β-Oxidation에 의한 γ-dodecalactone 생산에 이용되였고 GC 분석 결과, 시중에서 구매한 oleic acid로부터 얻어진 10-hydroxy stearic acid로부터 γ-dodecalactone 전환율은 78%이고 올리브유를 가수분해여 얻은 crude oleic acid로부터 얻어진 10-hydroxy stearic acid로부터 γ-dodecalactone 71% 정도 전환됨을 확인함.
4. 올리브유의 lipase 가수분해 산물로부터 확보한 hydroxy 지방산으로부터 γ-dodecalactone을 생산: Olive유를 Candida rugosa lipase (CRL)를 이용하여 가수분해한 후 S. maltophilia oleate hydratase를 반응 시켜 oleic acid를 10-hydroxystearic acid로 전환시키고 W. lipofer whole cells을 첨가하여 γ-dodecalactone을 생산. 40 g/L의 olive유로부터 25 g/L의 γ-dodecelactone을 생산함.
5. 홍화유의 lipase 가수분해 산물로부터 확보한 hydroxy 지방산으로부터 lactone 생산
홍화유를 Candida rugosa lipase (CRL)를 이용하여 가수분해한 후S. nitritireducens를 반응시켜 linoleic acid를 10-hydroxy-12(Z)-octadecenoic acid 등의 hydroxy 지방산으로부터 γ-lactone류를 생산함. 7.5 g/L의 홍화씨유로부터 1.88 g/L의 γ-dodecelactone을 생산하였고, 생산성은 235 mg L-1 h-1로 나타남.
6. 들기름의 lipase 가수분해 산물로부터 hydroxy 지방산 생산
들기름을 C. rugosa lipase (CRL)를 이용하여 가수분해한 후 Nostoc sp. lipoxygenase를 반응 시켜 50 g/L의 들기름(40 g/Lα-linolenic acid 함유)에서 34 g/L 9R-hydroperoxy-10E,12Z,15Z-octadecatrienoic acid 생산함.
7. 화장품 원료로 사용 시 생물전환으로 생산된 lactone은 정제가 필요 없음
정제된 생물 전환된 lactone은 화학 합성된 lactone과 차별성이 없으나 천연오일에 서 생산된 정제되지 않은 생물 전환된 lactone은 화학 합성된 lactone과 차별성이 있음.
라. 바이오 향료의 산업화 연구
1. Hydroxy 지방산 및 락톤류 분리 정제
(1) Hydroxy 지방산의 분리 정제: hydroxy fatty acids는 유기용매 저온 분별 정제법 또는 silicic acid open column chromatography를 사용하여 정제하였음. Methanol 정제법으로 83.9 g의 10-hydroxystearic acid를 70% 수율로 98% 이상의 순도로 얻음.
(2) γ-Lactones 정제 및 물질 동정:γ-lactones은 oil bath를 사용하여 환류냉각증류법을통해 각 해당 락톤을 63% 수율로 99% 순도 이상으로 정제하고 GC/MS로 동정함.
2. 바이오 향료 시제품 생산
(1) γ-Dodecalactone(51% 전환율),γ-decalactone(30% 이상 전환율),γ-dodecelactone(20% 이상 전환율), γ-butyrolactone(25% 이상 전환율), δ-decalactone(20% 이상 전환율) 시제품생산
(2) 10 L 발효조: 10-Hydroxy-12(Z)-octadecenoic acid로부터 γ-dodecelactone 생산: 30% 이상 전환율
(3) 올리브유로부터 γ-dodecalactone 혼합품 생산: 50% 이상 전환율
(4) 홍화유로부터 γ-dodecelactone 혼합품 생산
3. 경제성 분석
(1) Waltomyces lipofer에 의한 γ-dodecelactone 생산 원부재료비는 kg 당 20,469원으로 계산됨.
(2) Y. lipolytica에 의한 γ-lactone kg 당 생산 원부재료비: γ-decalactone는 82,260원γ-decelactone는 84,260원γ-dodecalactone는 174,075원γ-dodecelactone는 374,075원으로 계산됨.
(3) Y. lipolytica에 의한 γ-lactone kg당 생산단가: γ-decalactone는 611,545원γ-dodecalactone는 703,360원으로 추정됨.
(4) 화학합성한 판매가는 감마-락톤류가 30-40 $/kg이지만 천연유래 (동·식물로부터 직접추출) 제품의 경우 가격이 950 $/kg 정도이므로 경쟁력이 있음.
Ⅳ. Results
1) Production of hydroxy fatty acid
1. Production of hydroxy fatty acid by hydratase
(1) Lysinibacillus fusiformis hydratase produced 40 g/L 10-hydroxystearic acid from 40 g/L oleic acid after 3 h.
(2) Recombinant cells expressing Stenotrophomonas maltophilia hydratase produce
Ⅳ. Results
1) Production of hydroxy fatty acid
1. Production of hydroxy fatty acid by hydratase
(1) Lysinibacillus fusiformis hydratase produced 40 g/L 10-hydroxystearic acid from 40 g/L oleic acid after 3 h.
(2) Recombinant cells expressing Stenotrophomonas maltophilia hydratase produced 49 g/L 10-hydroxystearic acid from 50 g/L oleic acid after 4 h.
(3) Stenotrophomonas nitritireducens containing hydratase produced 15 g/L 10-hydroxy-12Z-octadecenoic acid 10-hydroxystearic acid from 20 g/L linoleic acid after 3 h.
(4) L. fusiformis oleate hydratase produced 13.5 g/L 10,12-dihydroxystearic acid from 15 g/L ricioleic acid after 3 h,
(5) Stenotrophomonas nitritireducens containing hydratase produced 16.4 g/L 10-hydroxy-12,15(Z,Z)- octadecadienoic acid from 22.5 g/L α-linolenic acid after 2 h.
(6) Lactobacillus acidophilus linoleate 13-hydratase produced 79 g/L 13-hydroxy-9Z-octadecenoic acid from 100 g/L linoleic acid after 3 h.
(7) L. acidophilus linoleate 13-hydratase produced 7.5 g/L 13-hydroxy-12,15 (Z,Z)-octadecadienoic acid from 15 g/L α-linolenic acid after 6 h.
2. Production of hydroxy fatty acid by diol synthase
(1) Recombinant cells expressing Aspergillus nidulans diol synthase produced 5.0 g/L 5,8-dihydroxy-9,12(Z,Z)-octadecadienoic acid from 5.0 g/L linoleic acid after 150 min.
(2) Recombinant cells expressing A. nidulans diol synthase produced 9.1 g/L 5,8-dihydroxy-9,12,15(Z,Z,Z)-octadecatrienoic acid from 12 g/L α-linolenic acid after 100 min.
(3) Recombinant cells expressing A. nidulans diol synthase produced 5.2 g/L 5,8-dihydroxy-9(Z)-octadecanoic acid from 12 g/L oleic acid after 60 min.
(4) Recombinant cells expressing A. nidulans diol synthase variant produced 1.8 g/L 8R-hydroperoxy-9,12(Z,Z)-octadecadienoic acid from 6 g/L linoleic acid after 60 min.
(5) Recombinant cells expressing Glomerella cingulate diol synthase produced 6.4 g/L 7,8-dihydroxy-9,12(Z,Z)-octadecadienoic acid from 14 g/L linoleic acid after 120 min.
(6) Recombinant cells expressing G. cingulate diol synthase produced 6.3 g/L 7,8-dihydroxy-9,12,15(Z,Z,Z)-octadecatrienoic acid from 14 g/L α-linolenic acid after 180 min.
(7) Recombinant cells expressing G. cingulate diol synthase produced 6.4 g/L 7,8-dihydroxy-9(Z)-octadecanoic acid from 14 g/L oleic acid after 150 min.
3. Production of hydroxy fatty acid by lipoxygenase
(1) Recombinant cells expressing Nostoc sp. lipoxygenase produced 37.6 g/L 9R-hydroxy-10E,12Z-octadecadienoic acid from 40 g/L linoleic acid after 60 min.
(2) Recombinant cells expressing Nostoc sp. lipoxygenase produced 38.4 g/L 9R-hydroperoxy-10E,12Z,15Z-octadecatrienoic acid from 40 g/L α-linolenic acid after 60 min.
(3) Burkholderia thailandensis lipoxygenase produced 21 g/L 13-hydroxy-9,11(Z,E)-octadecadienoic acid after 90 min.
2) Production of lactone
1. Waltomyces lipofer produced 45.7 g/L γ-dodecalactone from 60 g/L 10-hydroxystearic acid after 30 h.
2. β-Oxidation induction of W. lipofer by oleic acid: 22% increase in the yield of γ-dodecalactone from 10-hydroxystearic acid and 1.3-fold in the productivity. W. lipofer produced 28 g/L γ-decalactone from 60 g/L 12-hydroxystearic acid after 30 h. W. lipofer produced 12 g/L γ-butyrolactone from 60 g/L 10-hydroxydecanoic acid after 30h.
3. Candida boidinii produced 2.2 g/L γ-dodecelactone from 5 g/L 10-hydroxy-12(Z)-octadecenoic acid after 6 h.
4. Yarrowilia lipolytica produced 1 g/L δ-decalactonefrom 7.5 g/L 13-hydroxy-9-octadecenoic acid after 24 h.
5. Candida palmiolephila produced japonilure as Japanese beetle pheromone from 8-hydroxy-9-octadecenoic acid.
3) Development for production process of lactone from agricultural oil
1. Production of 25 g/L γ-dodecalactone from 40 g/L olive oil hydrolyzate with lipase treatment: Hydrolysis of olive oil by Aspergillus niger expressing CRL, Production of 10-hydroxy stearic acid from oleic acid by S. maltophilia oleate hydratase, Production of γ-dodecalactone by β-oxidation of W. lipofer whole cells.
2. Production of 1.88 g/L γ-dodecelactone from 7.5 g/L safflower oil hydrolyzate with lipase treatment: Hydrolysis of safflower oil by CRL, Production of 10-hydroxy-12(Z)-octadecenoic acid from linoleic acid by S. nitritireducens containing hydratase, Production of γ-dodecelactone by β-oxidation of C. boidinii whole cells.
3. Production of 34 g/L 9R-hydroperoxy-10E,12Z,15Z-octadecatrienoic acid from 50 g/L perilla oil hydrolyzate containing 40 g/Lα-linolenic acid with lipase treatment: Hydrolysis of perilla oil by CRL, Production of 10-hydroxy-12(Z)-octadecenoic acid from linoleic acid by Nostoc sp. lipoxygenase.
4. Recovery of biotransformed lactones were not needed for the use of cosmetic ingredient because biotransformed lactones were considered as natural lactone distinguished from chemically synthesized lactones.
4) Industrialization study of lactone
1. Recovery of hydroxy fatty acid and lactone
(1) Recovery of hydroxy fatty acid: Recovery of hydroxy fatty acid by low temperature fractional method or silicic acid open column chromatography. 10-Hydroxystearic acid was recovered with 98% purity and 70% yield by methanol method.
(2) Recovery of lactone: γ-Lactones was recovered with 99% purity and 63% yield using oil bath by circulating and cooling evaporation method.
2. Manufacture of test lactone samples
(1) Manufacture ofγ-dodecalactone (51% yield),γ-decalactone (above 30% yield),γ-dodecelactone (above 20% yield), γ-butyrolactone (above 25% yield), δ-decalactone (above 20% yield)
(2) Production of γ-dodecelactone from 10-Hydroxy-12(Z)-octadecenoic acid in a 10 L fermentor: above 30% yield
(3) Production of γ-dodecalactone mixture from olive oil: above 50% yield
3. Analysis of economic feasibility
(1) Raw material cost of γ-dodecelactone produced by W. lipofer: Estimation of 20,469 ₩/kg
(2) Raw material cost of γ-lactones produced by Y. lipolytica: Estimation of 82,260 ₩/kg forγ-decalactone, 84,260 ₩/kg forγ-decelactone, 174,075 ₩/kg forγ-dodecalactone, and 374,075 ₩/kg forγ-dodecelactone.
(3) Production cost of γ-lactones produced by Y. lipolytica: Estimation of 611,545 ₩/kg γ-decalactone and 703,360 ₩/kg forγ-dodecalactone.
(4) Selling price of chemically synthesized γ-lactones: 30-40 $/kg, Selling price of natural γ-lactones: 950 $/kg. Thus, biotransformed lactones exhibit cost competitiveness because they are near to natural γ-lactones.
 표
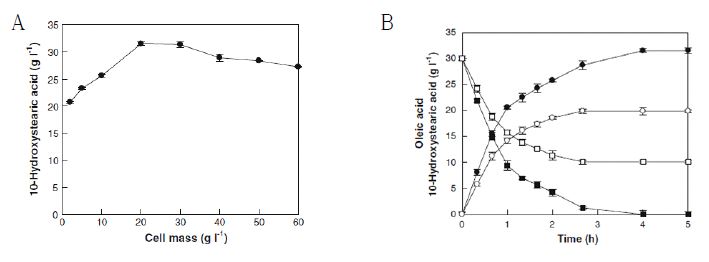
Fig. 2. a Effect of the cell concentration on the conversion of oleic acid to 10-hydroxystearic acid by whole cells of S. nitritireducens. b Time-courses for the conversion of oleic acid into 10-hydroxystearic acid by whole cells of S. nitritireducens under the optimum conditions in anaerobic and aerobic atmospheres. Oleic acid (filled circle) and (filled square) 10-hydroxystearic acid in anaerobic atmosphere and oleic acid (open circle) 10-hydroxystearic acid (open square) in aerobic atmosphere
표
Fig. 2. a Effect of the cell concentration on the conversion of oleic acid to 10-hydroxystearic acid by whole cells of S. nitritireducens. b Time-courses for the conversion of oleic acid into 10-hydroxystearic acid by whole cells of S. nitritireducens under the optimum conditions in anaerobic and aerobic atmospheres. Oleic acid (filled circle) and (filled square) 10-hydroxystearic acid in anaerobic atmosphere and oleic acid (open circle) 10-hydroxystearic acid (open square) in aerobic atmosphere
 표
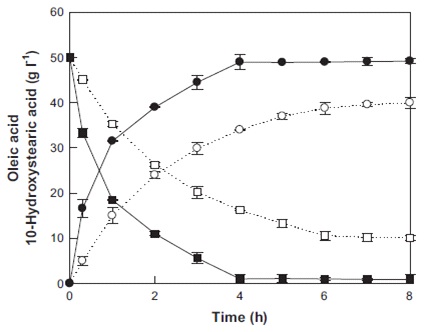
Fig. 7. Time-course reactions for 10-hydroxystearic acid production from oleic acid by whole cells of recombinant E. coli and wild-type S. maltophilia under the optimal conditions. 10-Hydroxystearic acid production (filled circle) from oleic acid (filled square) by whole cells of recombinant E. coli, and 10-hydroxystearic acid production (empty circle) from oleic acid (empty square) by whole cells of wild-type S. maltophilia.
표
Fig. 7. Time-course reactions for 10-hydroxystearic acid production from oleic acid by whole cells of recombinant E. coli and wild-type S. maltophilia under the optimal conditions. 10-Hydroxystearic acid production (filled circle) from oleic acid (filled square) by whole cells of recombinant E. coli, and 10-hydroxystearic acid production (empty circle) from oleic acid (empty square) by whole cells of wild-type S. maltophilia.
 표
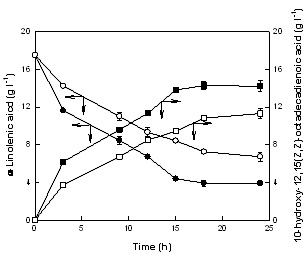
Fig. 13. Time-course reactions for the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid from α-linolenic acid by permeabilized cells and nonpermeabilized cells of S. maltophilia under the optimum conditions. The production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (■) from α-linolenic acid (●) by permeabilized cells and the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (□) from α-linolenic acid (○) by nonpermeabilized
표
Fig. 13. Time-course reactions for the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid from α-linolenic acid by permeabilized cells and nonpermeabilized cells of S. maltophilia under the optimum conditions. The production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (■) from α-linolenic acid (●) by permeabilized cells and the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (□) from α-linolenic acid (○) by nonpermeabilized
 표
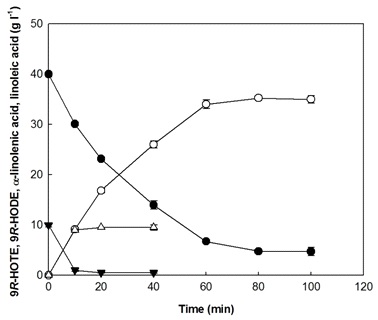
Fig. 10. Production of 9R-HOTE (empty circle) and 9R-HODE (empty triangle) from ALA (filled circle) and LA (filled inverse triangle) in PO hydrolyzate. The reactions were performed in a 500 mL baffled flask in 80 mL of 50 mM Tris-HCl buffer (pH 8.5) consisting of PO hydrolyzate, which contained 40 g/L ALA, 10 g/L LA, 15.3 g/L of other fatty acids, 5% (v/v) acetone, 0.2% (v/v) Tween 80, and 1 g/L purified 9R-LOX at 15 °C for 100 min with agitation at 250 rpm
표
Fig. 10. Production of 9R-HOTE (empty circle) and 9R-HODE (empty triangle) from ALA (filled circle) and LA (filled inverse triangle) in PO hydrolyzate. The reactions were performed in a 500 mL baffled flask in 80 mL of 50 mM Tris-HCl buffer (pH 8.5) consisting of PO hydrolyzate, which contained 40 g/L ALA, 10 g/L LA, 15.3 g/L of other fatty acids, 5% (v/v) acetone, 0.2% (v/v) Tween 80, and 1 g/L purified 9R-LOX at 15 °C for 100 min with agitation at 250 rpm
 표
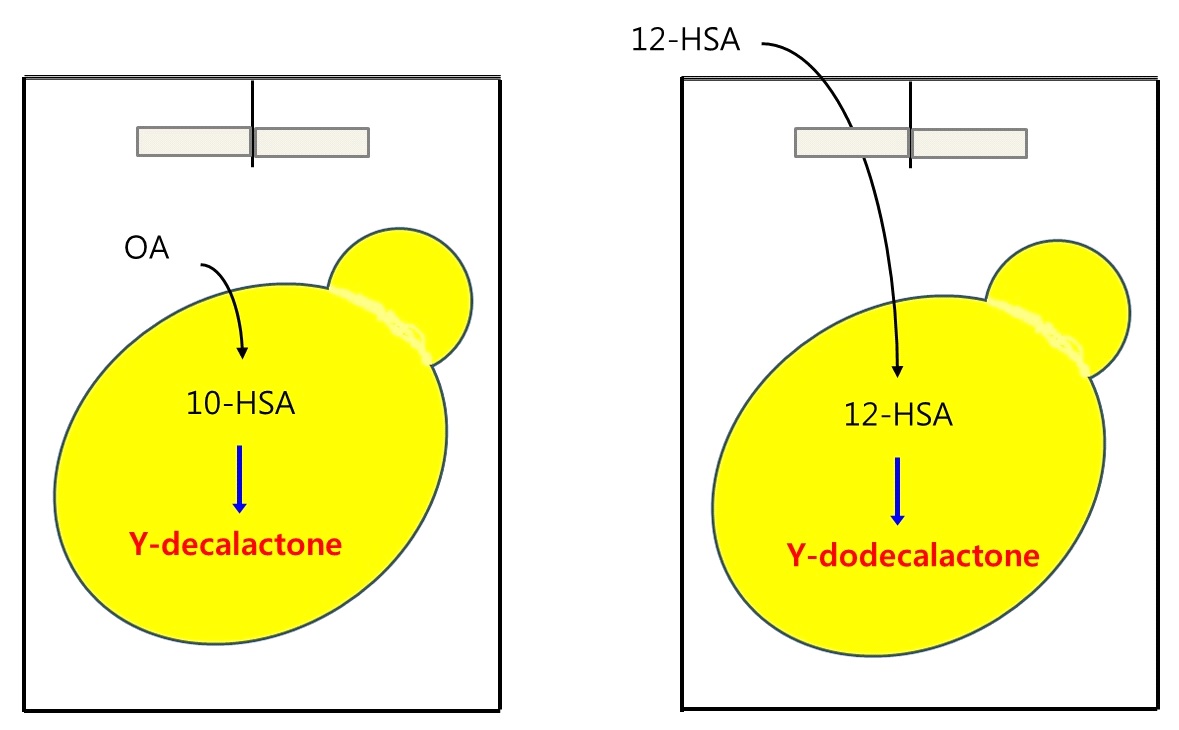
Fig. 17. Scenario of lactone production route by substrate or precursor supplementation. Lactone production from unsaturated fatty acid substrate (Left panel). γ-decalactone production from oleic acid(OA) via 10-hydroxystearic acid or γ-decelactone production from linoleic acid via 10-hydroxy-12Z-octadecenoic acid. Direct lactone production from hydroxy fatty acid (right panel). 12-Hydroxystearic acid (12-HSA) or ricinoleic acid to γ-dodecalactone or γ-dodecelactone
표
Fig. 17. Scenario of lactone production route by substrate or precursor supplementation. Lactone production from unsaturated fatty acid substrate (Left panel). γ-decalactone production from oleic acid(OA) via 10-hydroxystearic acid or γ-decelactone production from linoleic acid via 10-hydroxy-12Z-octadecenoic acid. Direct lactone production from hydroxy fatty acid (right panel). 12-Hydroxystearic acid (12-HSA) or ricinoleic acid to γ-dodecalactone or γ-dodecelactone
 표
Fig. 2. a Effect of the cell concentration on the conversion of oleic acid to 10-hydroxystearic acid by whole cells of S. nitritireducens. b Time-courses for the conversion of oleic acid into 10-hydroxystearic acid by whole cells of S. nitritireducens under the optimum conditions in anaerobic and aerobic atmospheres. Oleic acid (filled circle) and (filled square) 10-hydroxystearic acid in anaerobic atmosphere and oleic acid (open circle) 10-hydroxystearic acid (open square) in aerobic atmosphere
표
Fig. 2. a Effect of the cell concentration on the conversion of oleic acid to 10-hydroxystearic acid by whole cells of S. nitritireducens. b Time-courses for the conversion of oleic acid into 10-hydroxystearic acid by whole cells of S. nitritireducens under the optimum conditions in anaerobic and aerobic atmospheres. Oleic acid (filled circle) and (filled square) 10-hydroxystearic acid in anaerobic atmosphere and oleic acid (open circle) 10-hydroxystearic acid (open square) in aerobic atmosphere
 표
Fig. 7. Time-course reactions for 10-hydroxystearic acid production from oleic acid by whole cells of recombinant E. coli and wild-type S. maltophilia under the optimal conditions. 10-Hydroxystearic acid production (filled circle) from oleic acid (filled square) by whole cells of recombinant E. coli, and 10-hydroxystearic acid production (empty circle) from oleic acid (empty square) by whole cells of wild-type S. maltophilia.
표
Fig. 7. Time-course reactions for 10-hydroxystearic acid production from oleic acid by whole cells of recombinant E. coli and wild-type S. maltophilia under the optimal conditions. 10-Hydroxystearic acid production (filled circle) from oleic acid (filled square) by whole cells of recombinant E. coli, and 10-hydroxystearic acid production (empty circle) from oleic acid (empty square) by whole cells of wild-type S. maltophilia.
 표
Fig. 13. Time-course reactions for the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid from α-linolenic acid by permeabilized cells and nonpermeabilized cells of S. maltophilia under the optimum conditions. The production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (■) from α-linolenic acid (●) by permeabilized cells and the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (□) from α-linolenic acid (○) by nonpermeabilized
표
Fig. 13. Time-course reactions for the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid from α-linolenic acid by permeabilized cells and nonpermeabilized cells of S. maltophilia under the optimum conditions. The production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (■) from α-linolenic acid (●) by permeabilized cells and the production of 10-hydroxy-12,15(Z,Z)-octadecadienoic acid (□) from α-linolenic acid (○) by nonpermeabilized
 표
Fig. 10. Production of 9R-HOTE (empty circle) and 9R-HODE (empty triangle) from ALA (filled circle) and LA (filled inverse triangle) in PO hydrolyzate. The reactions were performed in a 500 mL baffled flask in 80 mL of 50 mM Tris-HCl buffer (pH 8.5) consisting of PO hydrolyzate, which contained 40 g/L ALA, 10 g/L LA, 15.3 g/L of other fatty acids, 5% (v/v) acetone, 0.2% (v/v) Tween 80, and 1 g/L purified 9R-LOX at 15 °C for 100 min with agitation at 250 rpm
표
Fig. 10. Production of 9R-HOTE (empty circle) and 9R-HODE (empty triangle) from ALA (filled circle) and LA (filled inverse triangle) in PO hydrolyzate. The reactions were performed in a 500 mL baffled flask in 80 mL of 50 mM Tris-HCl buffer (pH 8.5) consisting of PO hydrolyzate, which contained 40 g/L ALA, 10 g/L LA, 15.3 g/L of other fatty acids, 5% (v/v) acetone, 0.2% (v/v) Tween 80, and 1 g/L purified 9R-LOX at 15 °C for 100 min with agitation at 250 rpm
 표
Fig. 17. Scenario of lactone production route by substrate or precursor supplementation. Lactone production from unsaturated fatty acid substrate (Left panel). γ-decalactone production from oleic acid(OA) via 10-hydroxystearic acid or γ-decelactone production from linoleic acid via 10-hydroxy-12Z-octadecenoic acid. Direct lactone production from hydroxy fatty acid (right panel). 12-Hydroxystearic acid (12-HSA) or ricinoleic acid to γ-dodecalactone or γ-dodecelactone
표
Fig. 17. Scenario of lactone production route by substrate or precursor supplementation. Lactone production from unsaturated fatty acid substrate (Left panel). γ-decalactone production from oleic acid(OA) via 10-hydroxystearic acid or γ-decelactone production from linoleic acid via 10-hydroxy-12Z-octadecenoic acid. Direct lactone production from hydroxy fatty acid (right panel). 12-Hydroxystearic acid (12-HSA) or ricinoleic acid to γ-dodecalactone or γ-dodecelactone
| 과제명(ProjectTitle) : | - |
|---|---|
| 연구책임자(Manager) : | - |
| 과제기간(DetailSeriesProject) : | - |
| 총연구비 (DetailSeriesProject) : | - |
| 키워드(keyword) : | - |
| 과제수행기간(LeadAgency) : | - |
| 연구목표(Goal) : | - |
| 연구내용(Abstract) : | - |
| 기대효과(Effect) : | - |
Copyright KISTI. All Rights Reserved.

※ AI-Helper는 부적절한 답변을 할 수 있습니다.