최소 단어 이상 선택하여야 합니다.
최대 10 단어까지만 선택 가능합니다.
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
NTIS 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
DataON 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Edison 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Kafe 바로가기
| 주관연구기관 | 경상대학교 GyeongSang National University |
|---|---|
| 연구책임자 | 김석 |
| 참여연구자 | 정광면 , 김대근 , 한나심보리오 |
| 보고서유형 | 최종보고서 |
| 발행국가 | 대한민국 |
| 언어 | 한국어 |
| 발행년월 | 2015-09 |
| 과제시작연도 | 2014 |
| 주관부처 | 농림축산식품부 |
| 사업 관리 기관 | 농림수산식품기술기획평가원 |
| 등록번호 | TRKO201600000165 |
| 과제고유번호 | 1545008557 |
| 사업명 | 농생명산업기술개발 |
| DB 구축일자 | 2016-03-19 |
Ⅴ. 연구개발결과
1. 숙주특이 브루셀라 고면역원성 항원 발굴 및 고민감도 혈청학적 진단기법 개발
1). 숙주특이 브루셀라 고면역원성 균체항원 발굴 (28 종)
브루셀라 균체항원단백질에 대한 숙주의 감염시기별 최적 항원반응성을 나타내는 고면역원성 항원을 28종 발굴 (계획: 5종 이상) 하였으며 이들의 유전자적 특성 및 면역원성을 평가하였다.
2). 실험동물 대상 감염 시기별 고면역원성 항원 발굴
브루셀라 감염 마우스로부터의 혈청에 대한 항원 반응성을 보이는 브루셀라 균체항원단백질은 감염초기(10일)에는
Ⅴ. 연구개발결과
1. 숙주특이 브루셀라 고면역원성 항원 발굴 및 고민감도 혈청학적 진단기법 개발
1). 숙주특이 브루셀라 고면역원성 균체항원 발굴 (28 종)
브루셀라 균체항원단백질에 대한 숙주의 감염시기별 최적 항원반응성을 나타내는 고면역원성 항원을 28종 발굴 (계획: 5종 이상) 하였으며 이들의 유전자적 특성 및 면역원성을 평가하였다.
2). 실험동물 대상 감염 시기별 고면역원성 항원 발굴
브루셀라 감염 마우스로부터의 혈청에 대한 항원 반응성을 보이는 브루셀라 균체항원단백질은 감염초기(10일)에는 13개, 중기(30일)에는 24개, 말기(60일)에는 54개로 분석되었으며, 이들 중 감염초기의 1개, 중기의 3개, 말기의 8개는 비특이적 반응 및 Y. enterocolitica O:9과의 교차반응을 보여 배제시켜야 할 항원으로 평가되었다. 또한 실험동물 감염시기별 고면역원성 항원의 복합 조합 설정을 통해 감염초기와 중기의 공통반응 항원단백질은 1개, 감염초기와 말기는 5개, 감염중기와 말기는 8개로 나타났으며, 3가지 감염 시기 모두의 항원단백질은 인정되지 않았다. 따라서 비특이적 반응 및 교차반응을 배제시키고 감염시기별 높은 반응성을 가진 항원의 단위 및 복합 조합 설정을 통해 총 17개만이 실험동물 대상 감염 시기별 최적의 고면역원성 항원으로 평가되었다.
3). 목적동물 대상 감염 시기별 고면역원성 항원 발굴
브루셀라 감염 소로부터의 혈청에 대한 항원 반응성을 보이는 브루셀라 균체항원단백질은 감염초기(21일)에는 134개, 중기(49일)에는 110개, 말기(70일)에는 106개로 분석되었으며, 이들 중 13개의 비특이적 반응 및 13개의 Y. enterocolitica O:9 과의 교차반응이 나타나면서 배제시켜야 할 항원으로 평가되었다. 또한 목적동물 감염시기별 고면역원성 항원의 복합 조합 설정을 통해 감염초기와 중기의 공통반응 항원단백질은 19개, 감염초기와 말기는 10개, 감염중기와 말기는 4개로 나타났으며, 3가지 감염시기의 공통항원단백질은 74개로 평가되었다. 따라서 비특이적 반응 및 교차반응을 배제시키고 감염시기별 높은 반응성을 가진 항원의 단위 및 복합 조합 설정을 통해 총 55개만이 목적동물 대상 감염 시기별 최적의 고면역 원성 항원으로 평가되었다.
4). 실험동물과 목적동물의 고면역원성 항원의 최적 항원성 비교분석
브루셀라 균체항원단백질에 대한 숙주의 감염시기별 고면역원성 반응을 보인 최적 항원단백질은 실험동물(마우스)에서는 17개, 목적동물(소)에서는 55개로 평가되었다. 종합적으로 감염시기별 항원에 대해 실험동물(마우스)보다 목적동물(소)에서 더 높은 항원반응성(2.9배)을 나타내는 것으로 비교 평가되었으며, 이러한 결과는 Brucella abortus의 소에 대한 높은 숙주특이성으로 인해 기인된 것으로 판단된다. 실험동물(마우스) 감염시기별 최적 항원단백질들은 protein biosynthesis, proteolysis, metabolism, transcription 등에 관여하는 기능을 가진 단백질로 동정되었으며 일부는 아직 기능이 잘 밝혀지지 않은 putative uncharacterized protein으로 동정되어 앞으로 더 구체적인 기능규명연구가 요구된다고 판단된다. 비특이반응 및 교차반응을 모두 배제시킨 목적동물(소)과 실험동물(마우스)의 전체 반응성 공통항원단백질은 12개로 비교 평가되었으며 이 중 감염시기별 고면역원성 최적 항원반응으로 선별된 3개의 단백질(aldehyde dehydrogenase, malate dehydrogenase, superoxide dismutase, Cu-Zn)이 가장 진단적 가치 및 백신으로의 활용가치가 높을 것이라 판단된다.
5). 고면역원성 재조합 항원 28종 작제 및 면역원성 확인
브루셀라 고면역원성 균체항원 발굴: 제 1차년도에 수행된 고면역원성 항원 (9종)에 더하여 2차년도에 고면역원성 항원 19종 (Omp10, Omp19, Omp28, bfr, 0268 (Metal-dependent hydrolase), msrA, rocF, pgk, mdh (malate dehydrogenase), tsf, OsmC, ndk, asp, dps, YaeC, InPB, aspC, hypothetical protein, LivF, ndk 및 tbpA)을 발굴하여 총 28종에 대한 브루셀라 균의 고면역원성 재조합항원이 생산되었으며, 각 항원에 대한 면역 반응을 분석하여, 특이적인 면역반응이 나타나는 것을 확인하였다.
6). 숙주특이 고면역원성 재조합 항원의 세포독성 분석
브루셀라 고면역원성 균체항원 발굴: 제 1차년도에 수행된 고면역원성 항원 (9종)에 더하여 2차년도에 고면역원성 항원 19종을 발굴하여 총 28종에 대한 브루셀라 균의 고면역원성 재조합항원에 대한 세포 독성 평가 결과, 대부분이 세포독성이 없는 것으로 평가 됐으나, rocF, mdh 및 tsf 재조합단백의 경우 비교적 낮은 농도에서 (15 mg/ml) 독성이 인정되었다.
7). 고면역원성 재조합 항원을 이용한 ELISA 법 확립
각각의 재조합 항원을 이용하여, ELISA법을 수행해 TAT 결과와 비교해 본 결과, bfr, omp10, omp19, omp28 및 osmC에서 약 90% 이상의 민감도와 특이도를 보였고, 그 이외의 단백질은 반응성이 낮거나 민감도 특이도가 70% 미만에 그쳐, 위 5가지의 항원을 이용한 ELISA 방법 구축이 필요할 것으로 판단되었다.
8). 고면역원성 재조합 항원의 최적 조합 설정
각각의 재조합 항원을 이용하여, ELISA법을 수행해 TAT 결과와 비교하여, 우수한 결과를 도출한, bfr, omp10, omp19, omp28 및 osmC 5종의 조합을 수행해 본 결과, omp10, omp19, omp28항원의 경우 단일 항원의 사용에 비하여 조합을 하였을 때 민감도와 특이도가 95% 이상 증가되었으며, bfr 및 osmC는 단일 항원의 사용보다 낮은 민감도 (80% 미만)을 보여 단일 항원을 이용한 ELISA방법 개발에 적합 할 것으로 판단되었다.
9). 고면역원성 재조합 항원 대량생산 및 이를 이용한 간이 진단법 확립
재조합 항원 대량생산을 위해 pCold 및 pMal vector expression system을 이용한 대량생산기법이 확립되었음, 또한 이들 항원을 이용해 ELISA법을 수행해 TAT 결과와 비교해 우수한 결과를 도출한 bfr과 osmC재조합 항원을 이용하여 간이진단법 (Latex bead agglutination방법)을 수행 해 본 결과, bfr의 경우 특이도가 87.66%를 나타냈고, 민감도가 89.8%를 보였고 , osmC의 경우 특이도가 95.2%를 나타냈고, 민감도가 90.96%를 보여, 간이 진단기법의 개발이 가능할 것으로 판단 되었다. 또한, omp10, omp19, omp28항원을 이용한 Dip stick assay를 수행해본 결과 TAT와 비교하였을 때, TAT 음성혈청은 Dip stick assay 및 Sandwich Dip stick assay에서 음성을 보인 반면 TAT 양성 혈청은 rOmp 항원 조합을 이용한 ELISA에 비하여 특이도가 낮았지만, 현장 활용이 가능할 것으로 판단된다.
10). 개발된 진단방법의 경제성 평가
현재 브루셀라균 항원을 이용한 ELISA 방법은 유럽의 스바노바사 제품이 주요 진단킷트로 상용화 되어있으며, 96 sample 적용 기준 약 900$ 정도에 판매가 되고 있으나, 본 연구 과제를 통해 개발된 ELISA 진단기법의 경우 참여업체인 ㈜ 메디안 디노스틱과 평가를 해본 결과 96 sample 적용 기준 400$ 내외로 시장 공급이 가능할 것으로 평가되고 있으나, 이에 대한 구체적인 경제성 평가는 국내는 물론 전 세계적인 브루셀라 발생 상황, 판매 수요량 등에 따라 변화가 있을 것으로 판단되어져, 현 시점에서 확정하기는 다소 어려울 것으로 판단되며 보다 면밀한 분석이 요구된다.
2. 숙주특이 브루셀라 고면역원성 항원에 대한 면역반응 분석 및 진단적 가치 평가
1). 재조합 단백질의 생산 및 분석
제 1 세부과제에서 발굴된 9종의 숙주특이 브루셀라 pMal vector system을 이용한 고면역원성 재조합 단백질 (Omp10, Omp19, Omp28, OmpA, Omp2b, SodC, AspC, OsmC, DPS)과 pCold TF vector system을 이용한 9종의 고면역원성 재조합 단백질 (OMP28, mdh, tsf, rocF, 0628, Bfr, TbpA, OMP10, OMP19)에 대한 면역반응 분석 및 진단적 가치를 평가하기 위하여 고면역원성 재조합 단백질의 대량 정제를 실시하였으며, 분리 정제된 고면역원성 재조합 단백질들은 SDS-PAGE, Western blot, ELISA, in vitro, 그리고 in vivo 실험등에 각각 사용되었다.
2). 고면역원성 재조합 단백질을 이용한 혈청학적 분석
고면역원성 재조합 단백질을 분리 정제하여 야외가검혈청 및 인공감염우 혈청을 이용한 SDS-PAGE, Western blot, 그리고 ELISA 분석을 실시한 결과
(1) SDS-PAGE 및 Western blot
: pMal vector system을 이용한 재조합 단백질 중에서 OMP28이 Western blot 실험에서 야외가검혈청과 가장 높은 반응성을 나타내는 것을 확인하였다. 또한, pCold TF vector system을 이용한 재조합 단백질 중에서 OMP28은 야외가검혈청 및 인공감염우혈청을 이용한 Western blot에서 높은 민감도를 나타내었고 tsf는 인공감염우혈청을 이용한 Western blot에서 높은 민감도를 나타내었다. 반면에, 다른 단백질들은 양성혈청에 대한 민감도가 매우 낮게 나타났다.
(2) ELISA
: 고면역원성 재조합 단백질을 이용한 야외가검혈청 및 인공감염우 혈청과의 반응성을 검사하기 위해서 ELISA 기법을 이용하여 항원 및 혈청의 농도를 결정하였다. 이를 통하여 고면역원성 재조합 단백질을 이용한 혈청 민감도 검사를 실시하였고 OMP28 재조합 단백질이 가장 민감도가 높은 단백질로 확인되었다. 또한, ELISA 실험 결과에서 고면역원성 재조합 단백질들이 각각의 혈청 마다 다른 민감도를 나타내었다.
3). In vitro cytokines 생성 분석
6종의 고면역원성 재조합 단백질 (Omp10, Omp19, Omp28, OmpA, Omp2b, SodC)을 RAW 264.7 cell에 자극시킨 후 TNF-α 의 생성능을 확인한 결과 6종의 재조합 단백질 모두 자극 후 24시간부터 높은 생성능을 보이는 것을 확인하였다. 특히, Omp10 재조합 단백질의 TNF-α 생성능이 가장 높은 것으로 나타났다. 또한, 9종의 고면역원성 재조합 단백질 (OMP28, mdh, tsf, rocF, 0628, Bfr, TbpA, OMP10, OMP19)자극에 따른 면역매개물질(NO 및 cytokines) 발현을 분석한 결과 RAW 264.7 cell에서 TNF-α와 IL-6의 발현량이 증가하는 것을 확인하였다. 하지만, IL-1β, IL-12p70, IFN-γ의 생성은 검출량 이하였다. 특히, IL-6의 발현은 Th2 면역반응을 유도하는 물질로 잘 알려져 있으며 0628, Bfr, TbpA, OMP19 재조합 단백질 자극에 있어서는 초기부터 발현을 유도하는 것을 확인하였으며, rocF는 48시간부터 발현이 증가하는 것을 확인하였다. 이는 이들 고면역원성 재조합 단백질이 Th2 면역반응을 유도하는 것으로 판단된다.
4). In vivo 면역반응 유도능 분석
(1) Mouse
첫 번째 실험에서 6종의 고면역원성 재조합 단백질 (Omp10, Omp19, Omp28, OmpA, Omp2b, SodC)을 접종 후 혈청 내 항원 특이 항체 생성능 평가에서 IgM 생성능이 가장 높은 항원은 OmpA, Omp2b 이었으며, IgG 생성능이 가장 높은 항원은 Omp28, Omp2b 이었다. 세포성 면역을 확인한 고면역원성 항원을 마우스에 접종한 실험에서 접종된 마우스의 비장세포 중 항원 특이 항체 IgG 발현 세포 생성능이 높은 고면역원성 항원은 Omp28 이었으며 IL-4, INF-γ 발현 세포 생성능이 높은 항원은 Omp2b 이었다. 따라서 6종의 고면역원성 재조합 단백질을 통한 면역유도능 실험에서 면역반응이 가장 높게 관찰된 고면역원성 재조합 항원은 Omp28과 Omp2b 로 평가된다.
두 번째 실험에서 고면역원성 재조합 단백질 AspC, OsmC, DPS로 면역시킨 mouse 혈청을 이용한 ELISA test 결과 IgG1, IgG2a 그리고 cytokine 생성능이 높게 나타나는 것을 확인하였다.
세 번째 실험에서 Normal BALB/C mouse의 spleen으로부터 splenocytes를 분리하여 재조합 단백질로 자극시킨 결과 면역 초기 Th1 면역과 연관된 cytokines (IFN-γ와 IL-2)의 유도가 증가하는 것을 확인하였다. 반면에, Th2 면역과 관련된 cytokines (IL-4와 IL-5)의 발현은 확인할 수 없었다. 이는 재조합 단백질 자극이 naive한 splenocytes에 있어서 면역초기 세포성 면역반응을 유도하는 것으로 판단된다.
네 번째 실험에서 pCold TF vector system을 이용한 고면역원성 재조합 단백질 9종(OMP28, mdh, tsf, rocF, 0628, Bfr, TbpA, OMP10, OMP19)을 면역 후 면역기관 (spleen)에서의 면역반응여부를 평가하였다. BALB/C mouse를 고면역원성 재조합 단백질로 면역을 시킨 후 3, 7, 14, 28일째 혈청을 회수하여 ELISA를 통해 IgG 및 IgM의 항체 생성능을 확인한 결과 OMP28, 0628, Bfr, TbpA, OMP10, OMP19에 의한 항체 생성능은 매우 효율적으로 나타남을 확인하였다. 하지만, OMP10의 경우 IgM의 생성에 있어서 다른 재조합단백질들과 달리 시간경과에 따라 발현량이 증가하는 것을 확인하였다.
Mouse 면역 후 28일째 splenocyte를 회수하여 항체 또는 cytokine 발현 세포 수를 ELISpot으로 측정한 결과 0628, TbpA, OMP19, mdh 재조합 단백질에서 IgG 생성 세포 수가 유의하게 증가됐음을 확인하였고 OMP28, Bfr, OMP10은 유의성을 확인할 수 없었다. 그리고, Th1 면역에 관련된 IFN-γ 생성 세포 수에 있어서는 mdh와 tsf 재조합 단백질만이 유의하게 증가된 것을 확인하였고 Th2 면역에 관련된 IL-4 생성 세포 수에 있어서는 TbpA, mdh, tsf, rocF 재조합 단백질이 유의하게 증가하는 것을 확인하였다. 또한, in vivo 면역 후 면역기관에서 28일째 IFN-γ 생성 세포 수 보다 IL-4 생성 세포 수에 있어서 그발현량이 더 많은 것이 확인되었으며 이를 통하여 Th1 면역보다 Th2 면역반응의 증가를 유도하는 것으로 판단된다.
(2) Bovine
목적동물(소)의 PBMC에서 고면역원성 재조합 단백질 (Omp10, Omp19, Omp28, OmpA, Omp2b, SodC) 자극 후 cytokines 유전자 발현능 평가에서 3 가지 cytokines (IL-1β, IL-6, TNF-α) 유전자에서 발현증가율을 나타낸 항원은 Omp19, 2 가지 cytokines (IL-1β, TNF-α) 유전자 발현증가를 나타낸 항원은 Omp28 이었다. Apoptosis 유전자 발현능 평가에서 2가지 apoptosis (Bax, TLR4) 유전자 발현증가를 나타낸 항원은 Omp19, Omp28, OmpA 이었다.
또다른, 고면역원성 재조합 단백질 (OMP28, mdh, tsf, rocF, 0628)을 이용한 목적동물(소)의 PBMC에서 생성되는 cytokines의 발현을 비교분석한 결과 IL-6, IL12p40, IFN-γ, and TNF-α 4종류의 cytokine의 경우 시간의 변화에 따라 각각의 항원들에 의한 발현정도가 현저하게 차이가 나는 것을 확인하였으나 다른 3종류의 cytokine (iNOS, IL-1β, 및 IL-4)의 발현량은 시간에 따른 비교에서 크게 차이를 나타내지 않음을 확인하였다. 또한, cytokine들의 발현양상은 자극하는 항원의 양에 따라 다르게 나타났다.
5). 결론
이상의 실험결과를 바탕으로 고면역원성 재조합 단백질의 대량 정제기법을 확립할 수 있었고 in vitro 및 in vivo 면역유도능 실험을 통하여 고면역원성 재조합 단백질들이 Th1 면역보다는 Th2 면역유도능이 높게 나타나는 것을 확인하였다. 이러한 면역반응에 기초할 때에 본 실험에사용한 고면역원성 재조합 항원 중 OMP28, OMP2b, TbpA, mdh는 향후 브루셀라 진단용 후 보물질로 이용가능성이 매우 높으며, 특히 초기 감염우 검출을 위한 진단에 활용할 수 있을것으로 판단된다.
In the last few decades, various diagnostic test methods have been developed for the successful surveillance and control of Brucella infection. The standard diagnostic techniques for brucellosis include the isolation of causative organisms through bacterial culture, molecular assays for bacterial ge
In the last few decades, various diagnostic test methods have been developed for the successful surveillance and control of Brucella infection. The standard diagnostic techniques for brucellosis include the isolation of causative organisms through bacterial culture, molecular assays for bacterial genome detection, and serology through antibody detection. Bacterial culture, however, requires biosafety level 3 conditions and a skilled expert, while genomic detection is a rapid but limited technique for the recognition of active infection. Current serological assessments are more reliable and generally approved.
For the serological diagnosis of brucellosis in animals and humans, classical methods, such as the Rose Bengal test (RBT), agglutination test and enzyme linked immunosorbent assay (ELISA), have been widely established in various countries and are preferred in routine clinical practice. However, more enhanced sensitivity and specificity in the confirmatory diagnosis of brucellosis are still needed.
Consistent with these assessments, the diagnostic antigen used in classical serological tests is commonly derived from smooth lipopolysaccharide or O-polysaccharide as an immunodominant epitope for antibodies secreted in the humoral immune response. Despite the strong immunoreactivity of these common antigens, the specificity of LPS-based assays is assumed to be low, reflecting cross-reactions with other relevant bacteria, such as Y. enterocolitica O:9, which conserves the similar O-polysaccharide composition. Accordingly, diverse modifications in the diagnosis of brucellosis have been examined to overcome the limitations arising from the immune response against Brucella infection.
To determine reliable immunogenic proteins to detect Brucella abortus infection according to time course responses to aid in the appropriate management of this disease, proteomic identification through two-dimensional electrophoresis (2DE), followed by immunoblotting, revealed 13, 24, and 55 immunodominant B. abortus 544 proteins that were reactive to sera from experimentally infected mice at early (10 days), middle (30 days), and late (60 days) infection periods, respectively. After excluding several spots reactive to sera from Yersinia nterocolitica O:9-infected and non-infected mice, 17 of the 67 immunodominant proteins were identified through MALDI-TOF MS. Consequently, the identified proteins showed time course-dependent immunogenicity against Brucella infection.
In addition, this study examined novel immunogenic proteins that can be used to detect Brucella abortus infection or as an effective subcellular vaccine. In an immunoproteomic assay, 55 immunodominant proteins from B. abortus 544 were observed using two dimensional electrophoresis (2DE) and immunoblot profiles with antisera from B. abortus-infected cattle at the early (3 week), middle (7 week), and late (10 week) periods, after excluding protein spots reacting with antisera from Yersinia enterocolitica O:9-infected and non-infected cattle. Twenty-three selected immunodominant proteins whose spots were observed at all three infection periods were identified using MALDI-MS/MS. Most of these proteins identified by immunoblot and mass spectrometry were determined by their subcellular localization and predicted function.
Moreover, to develop alternative means that can distinguish between these two conditions without utilizing lipopolysaccharide (LPS), this study was an attempt to determine the efficacy of combined recombinant B. abortus outer membrane proteins (rOmps) and individual rOmps in the serodiagnosis of brucellosis by enzyme linked immunosorbent assay (ELISA), utilizing both that standard tube agglutination test (TAT)-positive and -negative serum samples from Korean native cattle. The results are very interesting and promising because the combined rOmp antigens used in the study were highly reactive with the TAT-positive serum samples. The combined rOmps sensitivity, specificity and accuracy were 215/232 (92.67%), 294/298 (98.66%) and 509/530 (96.04%), respectively. While these results are preliminary, the tests performed have very high potential in the serodiagnosis of brucellosis and likewise, the combined rOmps can be used for future vaccine production.
Moreover, we investigated the possible use of the B. abortus outer membrane protein A (OmpA), Omp10, Omp19, Omp28, Ndk, mdh, bfr, aspC, livF, tbp and several hypothetical proteinas a candidate recombinant proteins for serological diagnosis for bovine Brucellosis including latexbead agglutination assay, dip stick assay and wandsich dip stick assay application. After application, the results of these diagnostic tools was compared to those of TAT and Rose bengal, resulting that the sensitivity, specificity and accuracy was lower than those of ELISA using rOmps.
Eighteen recombinant proteins, nine proteins (Omp10, Omp19, Omp28, OmpA, Omp2b, SodC, AspC, OsmC, DPS) with pMal vector system and other nine proteins (OMP28, mdh, tsf, rocF, 0628, Bfr, TbpA, OMP10, OMP19) with pCold vector system, were expressed and purified by mass production system using His-spintrap column. Those proteins were used or the serological and immunological analysis by SDS-PAGE, Western blot, ELISA, and ELISpot. When the recombinant proteins were reacted with bovine positive sera, OMP28 showed high reactivity both Western blot and ELISA.
In the cytokine production analysis, production of TNF-α was increased after 24 hours in RAW 264.7 cell stimulated by six recombinant proteins (Omp10, Omp19, Omp28, OmpA, Omp2b, SodC). Of these proteins, Omp10 induced the highest production. Also, production f Nitric Oxide, TNF-α, and IL-6 were induced in RAW 264.7 cells stimulated with nine recombinant proteins (OMP28, mdh, tsf, rocF, 0628, Bfr, TbpA, OMP10, OMP19). However, IL-1β, IL-12p70, and IFN-γ were not detectable in this system. Production level of IL-6 were started in the increase of the production at 8 hours in RAW 264.7 cells stimulated with 0628, Bfr, TbpA, and OMP19.
Immune responses were analysed with the eighteen recombinant proteins in mice and/or bovine. In mouse, the proteins were intraperitoneally injected by 30 mg with complete adjuvant in BALB/C and booster injections were carried out with same amount of the roteins with incomplete adjuvant in 14 days. Sera were collected at 3, 7, 14, and 28 days after the injection. Then, production of IgG, IL-4, and IFN-γ were determined in the mouse sera using ELISA systems. Omp28 and Omp2b expressed with pMal vector system were showed high production rates of IgG, IL-4, and, IFN-γ.
OMP28, 0628, Bfr, TbpA, OMP10, and OMP19 expressed with pCold vector system induced the typical production of IgG and IgM in mice. However, OMP10 showed different pattern which was gradual increase of IgM production until 28 days.
In the analysis of immune induction of the proteins (OMP28, mdh, tsf, rocF, 0628, Bfr, TbpA, OMP10, OMP19) using cytokine production (IFN-g, IL-2, IL-4 and IL-5) in the naive splenocytes, production of IFN-γ and IL-2 were increased in 12 hours after the stimulation.
However, the immune induction showed different phenomenon in the immunized mice. Splenocytes were collected from mice immunized with nine recombinant proteins (OMP28, 0628, Bfr, TbpA, OMP10, OMP19, mdh, tsf, rocF) at 28 days after the first injection and the number of antigen secreting cell were analyzed using ELISpot after stimulation of the cells with the recombinant proteins. 0628, TbpA, OMP19, and mdh induced high number of IgG-secreting cells while mdh and tsf induced high number of IFN-γ-secreting cells. TbpA, mdh, tsf, and rocF induced high number of IL-4 secreting cells. Number of IL-4-secreting cells was higher than the number of IFN-γ-secreting cells (p<0.05). These results suggest that those antigens might induced Th2 immune system rather than Th1 immune system.
In the analysis of the induction of cytokine expression in bovine peripheral blood mononuclear cells after stimulation with eleven recombinant proteins (Omp10, Omp19, Omp28, OmpA, Omp2b, and SodC in pMal vector system; OMP28, mdh, tsf, rocF, and 0628 in pCold vector system). Omp28 and Omp19 expressed in pMal vector system induced high production of IL-1β and TNF-α. With the recombinant proteins expressed in pCold vector system, production of the cytokines (IL-6, IL12p40, IFN-γ, TNF-α, iNOS, IL-1β, and IL-4) was induced in time and dose-dependent manners. Especially, OmpA expressed with pMal vector system induced high expression of Bax and TLR4 genes, which are related with apoptosis.
Through those experiments, mass production system of recombinant proteins were established. Immune induction in naive and immunized immune cells were analyzed. Generally, Th2 immune system was induced by most of our recombinant proteins than Th1 immune system. The results of our experiment suggested that OMP28, Omp2b, TbpA, and mdh induced the Th2 immune system and might be candidates for diagnostic analysis of early brucellosis detection.
 표
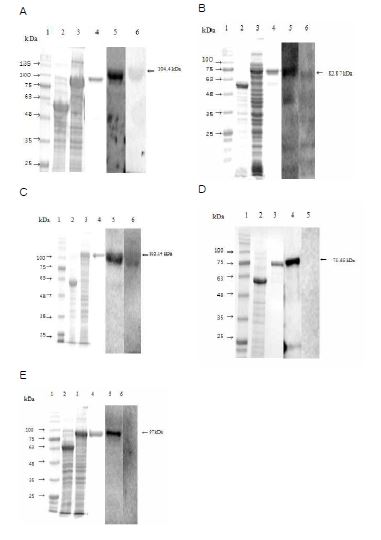
Fig. 41. 브루셀라 균체항원단백질 aspC, hypothetical protein, LivF, ndk 및 tbpA의 발현 및 감염우 혈청을 이용한 면역원성 분석. aspC(44 kDa)(A), hypothetical protein(22 kDa)(B), LivF(45 kDa)(C), ndk(15 kDa)(D) 및 tbpA (37 kDa)(E)이 pMal vector(60 kDa)에 재조합된 recombinant protein의 적정 크기(각각 104, 82, 105, 75 및 97 kDa)에서 발현이 유도됨을 확인할 수 있으며, 감염우 혈청을 이용한 Western blot을 수행해 본 결과 양성혈청과는 강한 반응을 보인반면 음성혈청과는 반응이 나타나지 않았음.
표
Fig. 41. 브루셀라 균체항원단백질 aspC, hypothetical protein, LivF, ndk 및 tbpA의 발현 및 감염우 혈청을 이용한 면역원성 분석. aspC(44 kDa)(A), hypothetical protein(22 kDa)(B), LivF(45 kDa)(C), ndk(15 kDa)(D) 및 tbpA (37 kDa)(E)이 pMal vector(60 kDa)에 재조합된 recombinant protein의 적정 크기(각각 104, 82, 105, 75 및 97 kDa)에서 발현이 유도됨을 확인할 수 있으며, 감염우 혈청을 이용한 Western blot을 수행해 본 결과 양성혈청과는 강한 반응을 보인반면 음성혈청과는 반응이 나타나지 않았음.
 표
Fig. 41. 브루셀라 균체항원단백질 aspC, hypothetical protein, LivF, ndk 및 tbpA의 발현 및 감염우 혈청을 이용한 면역원성 분석. aspC(44 kDa)(A), hypothetical protein(22 kDa)(B), LivF(45 kDa)(C), ndk(15 kDa)(D) 및 tbpA (37 kDa)(E)이 pMal vector(60 kDa)에 재조합된 recombinant protein의 적정 크기(각각 104, 82, 105, 75 및 97 kDa)에서 발현이 유도됨을 확인할 수 있으며, 감염우 혈청을 이용한 Western blot을 수행해 본 결과 양성혈청과는 강한 반응을 보인반면 음성혈청과는 반응이 나타나지 않았음.
표
Fig. 41. 브루셀라 균체항원단백질 aspC, hypothetical protein, LivF, ndk 및 tbpA의 발현 및 감염우 혈청을 이용한 면역원성 분석. aspC(44 kDa)(A), hypothetical protein(22 kDa)(B), LivF(45 kDa)(C), ndk(15 kDa)(D) 및 tbpA (37 kDa)(E)이 pMal vector(60 kDa)에 재조합된 recombinant protein의 적정 크기(각각 104, 82, 105, 75 및 97 kDa)에서 발현이 유도됨을 확인할 수 있으며, 감염우 혈청을 이용한 Western blot을 수행해 본 결과 양성혈청과는 강한 반응을 보인반면 음성혈청과는 반응이 나타나지 않았음.
| 과제명(ProjectTitle) : | - |
|---|---|
| 연구책임자(Manager) : | - |
| 과제기간(DetailSeriesProject) : | - |
| 총연구비 (DetailSeriesProject) : | - |
| 키워드(keyword) : | - |
| 과제수행기간(LeadAgency) : | - |
| 연구목표(Goal) : | - |
| 연구내용(Abstract) : | - |
| 기대효과(Effect) : | - |
Copyright KISTI. All Rights Reserved.

※ AI-Helper는 부적절한 답변을 할 수 있습니다.