최소 단어 이상 선택하여야 합니다.
최대 10 단어까지만 선택 가능합니다.
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
NTIS 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
DataON 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Edison 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Kafe 바로가기
| 주관연구기관 | 한국화학연구원 Korea Research Institute of Chemical Technology |
|---|---|
| 연구책임자 | 김용범 |
| 참여연구자 | 민병선 |
| 보고서유형 | 최종보고서 |
| 발행국가 | 대한민국 |
| 언어 | 한국어 |
| 발행년월 | 2020-11 |
| 과제시작연도 | 2020 |
| 주관부처 | 식품의약품안전처 Ministry of Food and Drug Safety |
| 과제관리전문기관 | 식품의약품안전평가원 National Institute of Food and Drug Safety Evaluation |
| 등록번호 | TRKO202100007704 |
| 과제고유번호 | 1475011744 |
| 사업명 | 안전성평가기술개발연구(R&D) |
| DB 구축일자 | 2021-07-31 |
| 키워드 | 천연물.물질분석.90일 반복투여독성.유전독성.단회투여독성.Natural medicine.Material analysis.90-day repeated dose toxicity.Genotoxicity.Single dose toxicity. |
세신의 열수추출물 및 분말의 독성을 평가하기 위해 국제적인 GLP 기준에 따라 유전독성, 단회투여 독성 및 90일 반복투여독성시험을 수행하여, 신뢰성 있는 안전성 자료 및 생약재의 인체위해성 배경자료를 확보하였다. 대상 천연물은 생약감별위원들이 표준 생약을 대한약전에 기초하여 감별하였다. 원료생약의 기준규격시험을 실시한 후 표준탕제법에 준하여 열탕 추출 후 동결건조하여 열수추출물을 확보하였고, 분쇄를 통한 분말을 확보하였다. HPLC을 이용하여 시료 중 성분분석 및 지표성분을 중심으로 안정성 확인 시험을 실시하였다.
세
세신의 열수추출물 및 분말의 독성을 평가하기 위해 국제적인 GLP 기준에 따라 유전독성, 단회투여 독성 및 90일 반복투여독성시험을 수행하여, 신뢰성 있는 안전성 자료 및 생약재의 인체위해성 배경자료를 확보하였다. 대상 천연물은 생약감별위원들이 표준 생약을 대한약전에 기초하여 감별하였다. 원료생약의 기준규격시험을 실시한 후 표준탕제법에 준하여 열탕 추출 후 동결건조하여 열수추출물을 확보하였고, 분쇄를 통한 분말을 확보하였다. HPLC을 이용하여 시료 중 성분분석 및 지표성분을 중심으로 안정성 확인 시험을 실시하였다.
세신 분말 및 열수추출물에 대한 독성을 조사하기 위하여 유전독성시험, 단회투여독성시험, 28일 반복 경구투여 용량결정시험 및 90일 반복경구투여 독성시험을 실시하였다. 유전독성시험결과, 세신 열수추출물에서 복귀돌연변이, 체외염색체이상 및 마우스 골수세포에서 소핵을 유발하지 않았다. 세신 분말의 경우, 복귀돌연변이 유발 및 체외염색체이상 시험에서 강한 양성으로 판정되었다. 일부 in vivo 유전독성시험에서 음성의 결과를 보였으나, in vitro 시험의 양성 결과가 대사활성계 처리에 관계 없이 양성반응을 보였고, 90일 반복투여 독성시험에서 전암 병변이 다수 관찰되는 점을 고려했을 때 세신 분말은 유전독성이 있는 것으로 판단된다. SD rat에 단회투여독성시험을 통해 개략의 치사량을 확인한 결과, 분말 및 열수추출물에서 개략의 치사량은 모두 5000 mg/kg을 초과하였다. SD rat에 0, 125, 250, 500, 2000 및 5000 mg/kg/day로 28일간 반복경구투여 하였고 해당시험에서 나온 결과를 바탕으로 용량을 설정하여 90일 반복 경구투여 독성시험을 국내외 GLP 기준을 적용하여 실험하였다. 평가항목으로 사망 및 일반증상 관찰, 체중 및 사료섭취량측정, 안검사, 뇨검사, 혈액학적검사, 혈액생화학적 검사, 호르분 분석, 부검소견 관찰, 장기중량측정 및 조직병리학적 검사를 실시하여 세신 열수추출물 및 분말에 대한 무독성량(no observed adverse effect level)을 설정하였다. 연구결과 세신 열수추출물의 경우 위의 조직소견(편평상피세포 과형성)을 근거로 무독성량은 암수 모두 2000 mg/kg/day로 판단되며, 세신 분말의 경우 간의 조직소견(간세포변이소 및 간세포샘종 등)을 근거로 무독성량은 수컷은 150mg/kg/day, 암컷의 경우 150 mg/kg/day 미만으로 판단된다.
(출처 : 요약문 7p)
As part of National Toxicology Program in Korea, we obtained safety data of herbal medicines by conducting genotoxicity, single-dose toxicity and 90-day repeat-dose toxicity tests according to international GLP standards. These natural products were distinguished by experts based on Korean Herbal Ph
As part of National Toxicology Program in Korea, we obtained safety data of herbal medicines by conducting genotoxicity, single-dose toxicity and 90-day repeat-dose toxicity tests according to international GLP standards. These natural products were distinguished by experts based on Korean Herbal Pharmacopoeia.
Standard specification test such as physicochemical, HPLC and contamination analysis were carried out in selected natural herbs and extracted according to standard hot water extraction by Korea Pharmocopoeia or powder and then freeze dried. Component and marker compound of the extract was mainly analyzed using HPLC method to confirm the stability.
To investigate the toxicity of powder or water extracts of Asiasaum Radix, genotoxicity, single dose toxicity, 28-day dose range finding and 90-day repeated toxicity studies were conducted. In genotoxicity, the result of extracted Asiasaum Radix did not increase the number of revertant colonies (Ames), the number of mataphases with structural and numerical aberrations (CA), the frequency of micronuclei in the bone marrow cells of ICR mice (MN). However, the result of powder Asiasaum Radix showed positive result of Ames and CA regardless of the application of the metabolic activation system and negative result of in vivo MN and Comet assay. Considering the result that positive result, which occurred regardless of the application of the metabolic activation system and precancerous lesions were observed in vitro test and 90-day repeated dose toxicity test, respectively, it is considered that powder Asiasaum Radix would have high potential of genotoxic risk. After single dose administration in SD rats, approximate lethal dose (ALD) was considered to be above 5000 mg/kg in the powder or water extracts forms. 28-day dose range finding study was performed at the dose levels of 0, 125, 250, 500, 2000 and 5000 mg/kg/day in SD rats by oral gavage. Based on these results, dose levels for 90-day repeated toxicity study were selected and the study was conducted by applying principles specified in national and international regulatory authorities GLP guidelines. Mortality, clinical observations, body weight measurement, food consumption, ophthalmic examination, urinalysis, hematology, clinical chemistry, hormone analysis, organ weight, macroscopic and microscopic examination were evaluated and no observed adverse effect level (NOAEL) for the powder or water extracts was determined. Based on the findings of stomach (squamous cell hyperplasia) or liver (focus of cellular alteration and hepatocyte adenoma, etc.), NOAEL was considered to be 2000 mg/kg/day in male and female rats in the water extracts form. and 150 mg/kg/day in male rats and below 150 mg/kg/day in female rats in the powder form, respectively.
(출처 : Summary 9p)
 표
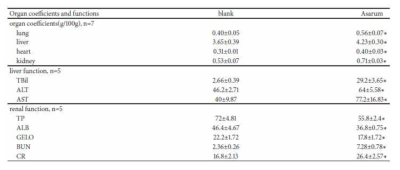
represent Asarum compare with blank p<0.05. To analyze the toxicity of Asarum to rats after intragastric administration with/without Asarum powders with the detection of organ coefficient, liver and kidney function. The results showed that the above data were all up-regulated after intragastric administration with Asarum powders. That may be induced by the toxicity of Asarum. The data were the means ± standard error of at least three independent experiments. Statistical significance was marked as ∗ while p<0.05. ∗represent the significant difference between the Asarum group and control group (p<0.05)
표
represent Asarum compare with blank p<0.05. To analyze the toxicity of Asarum to rats after intragastric administration with/without Asarum powders with the detection of organ coefficient, liver and kidney function. The results showed that the above data were all up-regulated after intragastric administration with Asarum powders. That may be induced by the toxicity of Asarum. The data were the means ± standard error of at least three independent experiments. Statistical significance was marked as ∗ while p<0.05. ∗represent the significant difference between the Asarum group and control group (p<0.05)
 표
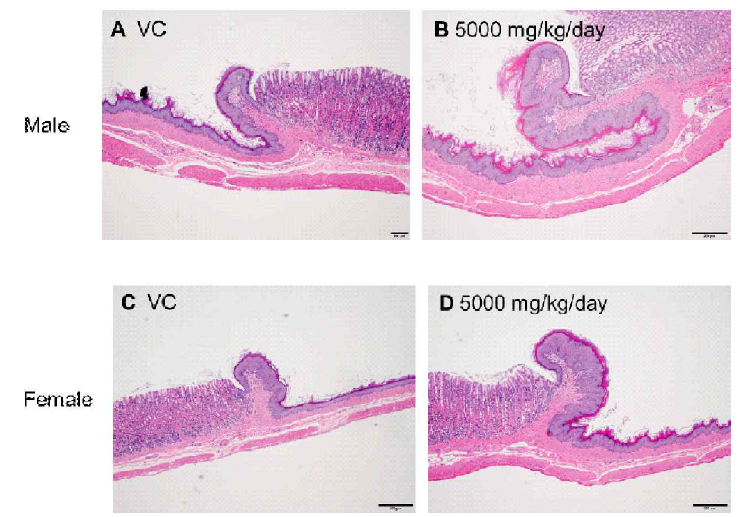
(A) Stomach from a male SD rat of control group (Main study). (B) Hyperplasia of squamous cells in stomach from a male 5000 mg/kg/day treatment group (Main study). (C) Stomach from a female SD rat of control group (Main study). (D) Hyperplasia of squamous cells in stomach from a female 5000 mg/kg/day treatment group (Main study). Scale bar, 200 μm; H&E
표
(A) Stomach from a male SD rat of control group (Main study). (B) Hyperplasia of squamous cells in stomach from a male 5000 mg/kg/day treatment group (Main study). (C) Stomach from a female SD rat of control group (Main study). (D) Hyperplasia of squamous cells in stomach from a female 5000 mg/kg/day treatment group (Main study). Scale bar, 200 μm; H&E
 표
represent Asarum compare with blank p<0.05. To analyze the toxicity of Asarum to rats after intragastric administration with/without Asarum powders with the detection of organ coefficient, liver and kidney function. The results showed that the above data were all up-regulated after intragastric administration with Asarum powders. That may be induced by the toxicity of Asarum. The data were the means ± standard error of at least three independent experiments. Statistical significance was marked as ∗ while p<0.05. ∗represent the significant difference between the Asarum group and control group (p<0.05)
표
represent Asarum compare with blank p<0.05. To analyze the toxicity of Asarum to rats after intragastric administration with/without Asarum powders with the detection of organ coefficient, liver and kidney function. The results showed that the above data were all up-regulated after intragastric administration with Asarum powders. That may be induced by the toxicity of Asarum. The data were the means ± standard error of at least three independent experiments. Statistical significance was marked as ∗ while p<0.05. ∗represent the significant difference between the Asarum group and control group (p<0.05)
 표
(A) Stomach from a male SD rat of control group (Main study). (B) Hyperplasia of squamous cells in stomach from a male 5000 mg/kg/day treatment group (Main study). (C) Stomach from a female SD rat of control group (Main study). (D) Hyperplasia of squamous cells in stomach from a female 5000 mg/kg/day treatment group (Main study). Scale bar, 200 μm; H&E
표
(A) Stomach from a male SD rat of control group (Main study). (B) Hyperplasia of squamous cells in stomach from a male 5000 mg/kg/day treatment group (Main study). (C) Stomach from a female SD rat of control group (Main study). (D) Hyperplasia of squamous cells in stomach from a female 5000 mg/kg/day treatment group (Main study). Scale bar, 200 μm; H&E
| 과제명(ProjectTitle) : | - |
|---|---|
| 연구책임자(Manager) : | - |
| 과제기간(DetailSeriesProject) : | - |
| 총연구비 (DetailSeriesProject) : | - |
| 키워드(keyword) : | - |
| 과제수행기간(LeadAgency) : | - |
| 연구목표(Goal) : | - |
| 연구내용(Abstract) : | - |
| 기대효과(Effect) : | - |
Copyright KISTI. All Rights Reserved.

※ AI-Helper는 부적절한 답변을 할 수 있습니다.