최소 단어 이상 선택하여야 합니다.
최대 10 단어까지만 선택 가능합니다.
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
NTIS 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
DataON 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Edison 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Kafe 바로가기
| 주관연구기관 | 바디텍메드 Boditechmed Inc |
|---|---|
| 연구책임자 | 최동환 |
| 참여연구자 | 김정란 , 심태선 , 김영균 |
| 보고서유형 | 최종보고서 |
| 발행국가 | 대한민국 |
| 언어 | 한국어 |
| 발행년월 | 2020-02 |
| 과제시작연도 | 2019 |
| 주관부처 | 보건복지부 [Ministry of Health & Welfare(MW)(MW) |
| 등록번호 | TRKO202100008824 |
| 과제고유번호 | 1465028635 |
| 사업명 | 감염병위기대응기술개발(R&D) |
| DB 구축일자 | 2021-09-04 |
| 키워드 | 잠복결핵감염.진단.항원 조합물.측방유동분석.인터페론감마.latent tuberculosis infection.diagnosis.antigen compound.lateral flow assay.ingerferon-gamma. |
□ 연구의 목적 및 내용
지금까지의 잠복결핵 감염의 진단용 제품은 100% 수입에 의존하고 있으며, 비용이 높고 검사과정이 복잡하며 고가의 장비를 이용해야만 사용 가능한 단점이 있음. 이를 극복하기 위하여 본 연구단은 일반 의료인이 저렴한 가격으로 간단한 검사과정을 통해 다수의 검체를 동시에 분석할 수 있는 자동화 검사 장비의 개발과 우수한 결핵 항원 조합물의 개발을 통해 기존 수입품의 성능에 버금가는 국산 잠복결핵감염 진단키트를 개발하고자함.
□ 연구개발성과
[기술] 본 제품의 개발을 위하여 결핵 퇴치사업의
□ 연구의 목적 및 내용
지금까지의 잠복결핵 감염의 진단용 제품은 100% 수입에 의존하고 있으며, 비용이 높고 검사과정이 복잡하며 고가의 장비를 이용해야만 사용 가능한 단점이 있음. 이를 극복하기 위하여 본 연구단은 일반 의료인이 저렴한 가격으로 간단한 검사과정을 통해 다수의 검체를 동시에 분석할 수 있는 자동화 검사 장비의 개발과 우수한 결핵 항원 조합물의 개발을 통해 기존 수입품의 성능에 버금가는 국산 잠복결핵감염 진단키트를 개발하고자함.
□ 연구개발성과
[기술] 본 제품의 개발을 위하여 결핵 퇴치사업의 중심인 대한결핵협회·결핵연구원과 “한국형 고효율 결핵감염 진단 기술의 개발 및 사업협력”을 위한 업무협약을 맺고(2017년 5월 31일)국내 채혈관 제조사(에이비메디컬(주)), 병원(아산병원)과 연계하여 본 국책연구사업(한국보건산업진흥원)을 통해 신속히 제품 국산화와 상용화를 이룰 수 있었다. 특히, 결핵연구원의 잠복결핵감염 진단용 특허들 중 “결핵감염 진단용 항원 조합물 관련 기술 및 노하우”의 전용 실시권을 얻어(2018년 6월 14일) 개발한 항원 채혈관은 기존 수입산 항원 채혈관과 동등한 성능을 가지고 있음을 임상성능 평가를 완료하였으며 카트리지와 함께 국내 인허가 및 상업화를 본격화 중이다.
[제품] 본 과제의 결과물인 ichroma™ IGRA-TB는 현재 국내 및 세계 시장을 독점하고 있는 ELISA 방식의 제품과 달리 15분 이내에 신속히 잠복결핵 유무를 측정할 수 있는 래피드 방식의 잠복결핵 진단 제품으로 바디텍메드(주)의 독자적인 초고감도 진단기기인 ichroma II 또는 전자동화 장비인 ichroma-50을 사용하여 신속하게 잠복결핵 감염의 여부 판정이 가능한 세계 최초의 제품이다.
[허가] 진진단기기는 전기적 안전 및 EMC 인증을 획득하고 식약처 신고를 완료하였으며 진단카트리지는 다기관임상시험(서울아산병원, 강동성심병원, 강원대학교병원, 중앙대학교병원)을 통해 허가를 위한 임상시험을 완료하였으며 결과를 논문화 중임. 동시에, 식약처 승인(제허 19-555 호,제신 17-1235 호)을 받아 해외 임상평가 및 판매 중이며 2020년 상반기에 내수를 위한 제조 및 판매 허가를 취득할 예정이다.
□ 연구개발성과의 활용계획 (기대효과)
[의의] ichroma™ IGRA-TB는 산업체-학교(대학병원)-연구원이 상호 협력하여 순수 국내의 기술력으로 개발한 합작품으로 기존 수입품에 버금가는 성능으로 수입대체 및 국부 유출 방지효과를 극대화할 수 있었으며, 저비용의 국산제품으로 소규모 검사기관 및 전문 검사인력이 없는 검사기관에서도 간단한 시험자 교육을 통하여 정확한 검사 결과를 얻을 수 있으므로 결핵퇴치를 위한 공공사업의 효율을 극대화할 수 있다.
[국내] 잠복결핵 진단제품의 국산화로 결핵예방을 위해 정부에서 추진하고 있는 “New 2020 plan”에 맞춰 어디에서든 잠복결핵 진단이 가능하게 되면서 본 제품이 “결핵 안심국가 실행계획“실천을 통한 결핵 전파의 사전 차단에 유용히 활용될 수 있을 것으로 예상하고 있음. 이를 위해 2020년 조달청의 [기술혁신 시제품 시험구매 사업]을 통해 병무청 등의 잠복결핵 위탁검사 용역사업에 참여를 추진중이다.
[임상성능평가] 국내 및 국외(FIND TB program, STOP TB Partnership, 아프리카, 유럽 등)에서 지역 판매자가 진행하는 성능평가용 임상시험을 추진 및 진행하고 있으며 높은 만족도를 보이고 있으므로 추후 성능 평과 결과가 실제 판매로도 연결될 수 있도록 긴밀히 협조 중이다.
[파생상품] 사용자 편의성을 위해 정맥혈 대신 말초혈을, 세 개의 채혈관 대신 한 개의 채혈관만을 사용하는 진일보한 파생상품의 개발을 추진하고 있으며 현지 판매자들에게는 개선품의 컨셉만으로도 매우 긍정적인 기대의 반응을 이끌어내고 있다.
(출처 : 국문 요약문 4p)
□ Purpose&Contents
Until now, diagnostic products of latent tuberculosis infections depend on 100% import, and have disadvantages such as high cost, complicated test process, and use of expensive equipment. In order to overcome this problem, we will develop an automated test equipment that allows
□ Purpose&Contents
Until now, diagnostic products of latent tuberculosis infections depend on 100% import, and have disadvantages such as high cost, complicated test process, and use of expensive equipment. In order to overcome this problem, we will develop an automated test equipment that allows a general practitioner to analyze multiple samples at the same time through a simple test process at a low price. At the same time, we will develop a diagnostic kit for latent TB infection that is comparable to the performance of existing imports by developing a superior TB antigen combination.
□ Results
[Technologies] For the development of this product, we entered into a business agreement with the Korea Tuberculosis Association and Tuberculosis Institute, the center of the tuberculosis eradication project, for the development and business cooperation of Korean high-efficiency tuberculosis infection diagnosis technology (31 May 2017). In cooperation with the blood vessel manufacturer (AB Medical) and the hospital (Asan Hospital), this national research project (Korea Health Industry Development Institute, KHIDI) was able to quickly localize and commercialize the product.
In particular, the antigen collection tube developed under the exclusive license of “Technology and know-how related to antigen combination for diagnosis of tuberculosis infection” among the patents for diagnosis of latent tuberculosis infection of the TB Research Institute (June 14, 2018) is equivalent to the existing imported antigen collection tube. The clinical performance evaluation has been completed and the domestic license and commercialization with cartridges are in full swing.
[Products] ichroma ™ IGRA-TB, the result of this task, is a rapid latent tuberculosis diagnostic product that can rapidly detect latent tuberculosis within 15 minutes, unlike ELISA-type products that currently dominate the domestic and global markets. It is the world's first product that can quickly determine whether latent tuberculosis infection is made using ichroma II, BoditechMed's unique high-sensitivity diagnostic device, or ichroma-50, a fully automated device.
[Permits] The diagnostic device has obtained the electrical safety and EMC certification and completed the KFDA notification. The diagnostic cartridge has completed clinical trials for approval through multi-center clinical trials (Seoul Asan Hospital, Gangdong Sacred Heart Hospital, Kangwon National University Hospital, Chung-Ang University Hospital) and the results are being documented.
At the same time, KFDA approvals (No. 19-555 and No. 17-1235) have been approved for overseas clinical evaluation and sales, and the first half of 2020 is expected to obtain a manufacturing and marketing license for domestic demand
□ Expected Contribution
[Significances] ichroma ™ IGRA-TB is a joint product developed by industry-school (university hospital) -researcher and developed with pure domestic technology. Its performance is comparable to that of existing imports, and it can maximize import substitution and local spill prevention effects. As a domestic product, accurate test results can be obtained through simple tester training even in small test institutes and test institutes without specialized test personnel, thus maximizing the efficiency of public works to combat tuberculosis.
[Domestic] The localization of latent tuberculosis diagnostic products enables the diagnosis of latent tuberculosis anywhere in accordance with the government's “New 2020 plan” to prevent tuberculosis. Therefore, It is expected to very useful for proactive blocking the latent TB. To this end, it is pursuing to participate in the latent tuberculosis consignment inspection service project by the military service office through the Procurement Agency's [Technical Innovation Prototype Procurement Project] in 2020.
[Clinical evaluation] In the domestic and foreign countries (FIND TB program, STOP TB Partnership, Africa, Europe, etc.), we are conducting and conducting clinical trials for performance evaluation conducted by local sellers and show high satisfaction. We are working closely together to lead to sales.
[Derivative Products] For the convenience of users, we are developing advanced derivative products that use peripheral blood(Finger blood) instead of venous blood and only one blood tube instead of three blood vessels. This is a very positive response from local sellers with the concept of refinement alone.
(출처 : SUMMARY 5p)
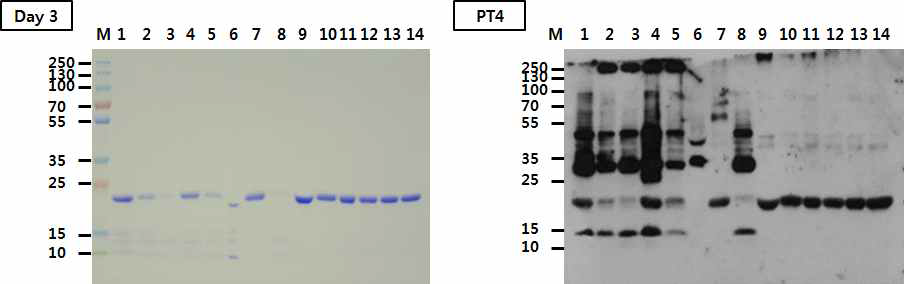 표
37℃에서 융합물질에 대한 ESAT6 단백질 안정화 반응 SDS-PAGE와 western blot. M: molecular weight markers, lane 1: pET21a-ESAT6, lane 2: 33.3 mM Trehalose, lane 3: 16.7 mM Glucose, lane 4: 16.7 mM Sucrose, lane 5: 33.3 mM Mannitol, lane 6: 6.7 % PEG, lane 7: 33.3 mM L-arginine, lane 8: 1.3 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +1 % PEG, lane 10: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 11: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 12: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 13: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose, lane 14: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol
표
37℃에서 융합물질에 대한 ESAT6 단백질 안정화 반응 SDS-PAGE와 western blot. M: molecular weight markers, lane 1: pET21a-ESAT6, lane 2: 33.3 mM Trehalose, lane 3: 16.7 mM Glucose, lane 4: 16.7 mM Sucrose, lane 5: 33.3 mM Mannitol, lane 6: 6.7 % PEG, lane 7: 33.3 mM L-arginine, lane 8: 1.3 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +1 % PEG, lane 10: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 11: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 12: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 13: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose, lane 14: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol
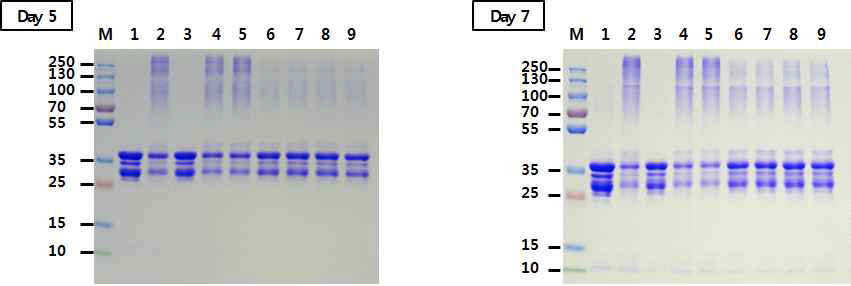 표
37℃에서 융합물질에 대한 CFP10 단백질 안정화 반응의 SDS-PAGE. M: molecular weight markers, lane 1: pGEX4T-CFP10, lane 2: 20 mM L-arginine, lane 3: 10 mM L-glutamine, lane 4: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 5: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 6: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose + 10 mM L-glutamine, lane 7: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose + 10 mM L-glutamine, lane 8: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM L-glutamine
표
37℃에서 융합물질에 대한 CFP10 단백질 안정화 반응의 SDS-PAGE. M: molecular weight markers, lane 1: pGEX4T-CFP10, lane 2: 20 mM L-arginine, lane 3: 10 mM L-glutamine, lane 4: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 5: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 6: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose + 10 mM L-glutamine, lane 7: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose + 10 mM L-glutamine, lane 8: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM L-glutamine
 표
37℃에서 융합물질에 대한 ESAT6 단백질 안정화 반응 SDS-PAGE와 western blot. M: molecular weight markers, lane 1: pET21a-ESAT6, lane 2: 33.3 mM Trehalose, lane 3: 16.7 mM Glucose, lane 4: 16.7 mM Sucrose, lane 5: 33.3 mM Mannitol, lane 6: 6.7 % PEG, lane 7: 33.3 mM L-arginine, lane 8: 1.3 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +1 % PEG, lane 10: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 11: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 12: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 13: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose, lane 14: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol
표
37℃에서 융합물질에 대한 ESAT6 단백질 안정화 반응 SDS-PAGE와 western blot. M: molecular weight markers, lane 1: pET21a-ESAT6, lane 2: 33.3 mM Trehalose, lane 3: 16.7 mM Glucose, lane 4: 16.7 mM Sucrose, lane 5: 33.3 mM Mannitol, lane 6: 6.7 % PEG, lane 7: 33.3 mM L-arginine, lane 8: 1.3 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +1 % PEG, lane 10: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 11: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 12: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 13: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose, lane 14: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol
 표
37℃에서 융합물질에 대한 CFP10 단백질 안정화 반응의 SDS-PAGE. M: molecular weight markers, lane 1: pGEX4T-CFP10, lane 2: 20 mM L-arginine, lane 3: 10 mM L-glutamine, lane 4: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 5: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 6: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose + 10 mM L-glutamine, lane 7: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose + 10 mM L-glutamine, lane 8: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM L-glutamine
표
37℃에서 융합물질에 대한 CFP10 단백질 안정화 반응의 SDS-PAGE. M: molecular weight markers, lane 1: pGEX4T-CFP10, lane 2: 20 mM L-arginine, lane 3: 10 mM L-glutamine, lane 4: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose, lane 5: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose, lane 6: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM Sucrose + 10 mM L-glutamine, lane 7: 20 mM L-arginine + 10 mM Trehalose + 10 mM Sucrose + 10 mM L-glutamine, lane 8: 20 mM L-arginine + 10 mM Mannitol + 10 mM Sucrose +10 mM L-glutamine, lane 9: 20 mM L-arginine + 10 mM Trehalose + 10 mM Mannitol + 10 mM L-glutamine
| 과제명(ProjectTitle) : | - |
|---|---|
| 연구책임자(Manager) : | - |
| 과제기간(DetailSeriesProject) : | - |
| 총연구비 (DetailSeriesProject) : | - |
| 키워드(keyword) : | - |
| 과제수행기간(LeadAgency) : | - |
| 연구목표(Goal) : | - |
| 연구내용(Abstract) : | - |
| 기대효과(Effect) : | - |
Copyright KISTI. All Rights Reserved.

※ AI-Helper는 부적절한 답변을 할 수 있습니다.