최소 단어 이상 선택하여야 합니다.
최대 10 단어까지만 선택 가능합니다.
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
NTIS 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
DataON 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Edison 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Kafe 바로가기
| 주관연구기관 | 가톨릭대학교 Catholic University of Korea |
|---|---|
| 연구책임자 | 조현일 |
| 참여연구자 | 이상은 , 신아리 |
| 보고서유형 | 최종보고서 |
| 발행국가 | 대한민국 |
| 언어 | 한국어 |
| 발행년월 | 2018-12 |
| 과제시작연도 | 2017 |
| 주관부처 | 보건복지부 [Ministry of Health & Welfare(MW)(MW) |
| 과제관리전문기관 | 한국보건산업진흥원 Korea Health Industry Development Institute |
| 등록번호 | TRKO202200008605 |
| 과제고유번호 | 1465024095 |
| 사업명 | 질환극복기술개발 |
| DB 구축일자 | 2022-09-24 |
| 키워드 | 종양백신 .종양회피. 이형-백신주입. 병용-치료. 항종양효과cancer vaccine .tumor escape. heterologous vaccination.combined therapy .antitumor effect |
연구의 목적 및 내용
본 과제는 이형-백신주입 (heterogeous vaccination) 전략을 극대화하여 종양의 면역회피 (immune escape) 기전을 극복하는 간편성⋅범용성이 향상된 최적의 종양백신을 개발하여 고-친화성 다-항원-특이 면역능을 유도하기 위한 병용-면역치료 전략의 항-종양효과를 검증함으로서 종양백신-기반 면역치료제 개발의 신규 원천기술을 확립하여 중개중점 연구로의 확장을 목표로 함. 구체적으로,
◦최적의 이형-백신 주입 (heterogeous vaccination) 전략을 위한 항-종양백신 확인
연구의 목적 및 내용
본 과제는 이형-백신주입 (heterogeous vaccination) 전략을 극대화하여 종양의 면역회피 (immune escape) 기전을 극복하는 간편성⋅범용성이 향상된 최적의 종양백신을 개발하여 고-친화성 다-항원-특이 면역능을 유도하기 위한 병용-면역치료 전략의 항-종양효과를 검증함으로서 종양백신-기반 면역치료제 개발의 신규 원천기술을 확립하여 중개중점 연구로의 확장을 목표로 함. 구체적으로,
◦최적의 이형-백신 주입 (heterogeous vaccination) 전략을 위한 항-종양백신 확인
◦다-항원 (multi-antigen)-특이 고-친화성 T 세포 유도 및 병용-면역치료 항-종양효과 조사
◦종양환경 T 세포의 면역회피 기전 극복 전략 조사 및 임상적용 가능성 검증
연구개발 성과
◦CD70, CD80, OX40L, 4-1BBL 및 IL12, IL21와 케모카인 (CXCL9/10)-수용체 (CXCR3)를 발현하는 T 세포 또는 B 세포를 이용하거나, 핵산 (DNA)-기반 백신을 이용하여 이형-백신주입 전략의 항종양능 유도와 수지상세포-대체 종양백신으로 이용 가능성을 비교/검증함.
◦T 세포-활성화의 anti-4.1BB, anti-OX40 항체를 이용한 이형-백신조합의 가능성 및 T 세포-입양주입 후 anti-CD40/anti-OX40/anti-4-1BB 항체에 의한 T 세포의 증식 및 항원-특이 T 세포면역능을 확인함.
◦수지상세포-백신/펩타이드-백신 이형-백신 전략의 Poly-IC (TLR3-L)-대체 TLR-결합 리간드 [CpG (TLR9-L), LPS (TLR4-L), Pam2CSk4 (TLR2-L), Gardiquimod (GDQ; TLR7-L)] 분자를 사용하여 TLR-매개 내재면역계-활성화 신호전달의 차이에 의한 항원-특이 CD8 T 세포유도능을 비교/분석함.
◦흑색종양-특이 항원결정기 Trp1455, Trp2180, gp10025를 furin-sensitive linker (RVKR)로 연결한 DNA를 이용하여 다-항원-특이 항종양 면역능을 유도함.
◦다-항원-기반 항원구상을 위해 다수 종양에서 발현하는 polo-like kinase-1 (PLK1) 항원-유래 항원결정기를 이용하여 혈액암, 간암, 흑색종양 모델에서 다-항원-특이 항종양 면역능 유도 및 면역검문 PD-1/PD-L1 저해-병용 항종양-항진 기전을 확인함.
◦골다공증 및 일부 혈액암의 항암제로 사용되는 Zoledronate 및 Rapamycin을 병용한 이형-종양백신 전략의 향상된 항종양효과를 마우스 혈액암 및 고형암 (흑색종/대장암) 모델에서 검증하고 항종양 기전을 조사하였음.
◦유전자-변형 (gene-engineered) T 세포를 이용한 입양-세포 주입/종양백신 전략 연구를 위해 흑색종-특이 항원 gp10025–표적 TCR 유전자를 이용한 TCR-변형 T 세포를 생산하여 항원-표적능을 확인함.
◦이형-백신 전략에서 T 세포의 증식을 유도하는 IL-2/anti-IL2 복합체 및 면역검문 PD-1/PD-L1 저해-병용 전략과 항암제 Zoledronate-병용에 의한 항종양능 항진 (synergy) 효과 및 종양미세 환경의 항원-특이 T 세포의 특성을 검증함.
◦HLA-A2 Tg마우스에서 이형-백신 전략에 의해 HLA-A2-양성 사람종양세포를 인식하는 고-친화성 (high avidity) 항원-특이 CD8 T 세포를 유도하고, HLA-A2 Tg마우스-종양모델을 위한 HLA-A2-발현 흑색종 및 혈액암세포주를 확립하여 이형-종양백신 전략의 항종양효과를 확인함.
연구개발 성과의 활용계획 (기대효과)
◦미래 의약 (Futuristic Medicine)로 항-종양백신 면역치료 글로벌 시장에서 경쟁력 확보
◦고-효능 종양백신 개발 및 병용-면역치료법의 임상적용을 위한 기본 정보 축적
◦종양의 면역회피 (immune escape) 기전을 극복하는 범용-면역치료법 개발 자료로 활용
◦기성품 (off-the-shelf) 단계의 상용화 항-종양백신 개발의 핵심 원천기술 제공
◦면역치료제 개발의 국제 공동연구의 기초 자료로 활용
(출처 : 요약문 12p)
Purpose&Contents
Our final goal is to develop a optimal cancer immunotherapeutic strategy capable of circumventing the cancer immune escape in tumor microenvironments and expanding its applicability into clinic. To achieve this goal, we evaluate therapeutic efficacies of combined heterogeous vacc
Purpose&Contents
Our final goal is to develop a optimal cancer immunotherapeutic strategy capable of circumventing the cancer immune escape in tumor microenvironments and expanding its applicability into clinic. To achieve this goal, we evaluate therapeutic efficacies of combined heterogeous vaccination regime, which are able to enhance multi-antigenspecific high-avidity T-cells and memory T-cell responses as translational pre-clinical studies.
Results
For improving the limitation of DC-based vaccine for clinical use, we have evaluated heterologous vaccination strategies with antigen-loaded T-cells or B-cells, which were genetically modified with CD70, CD80, OX40L, and 4-1BBL either alone or together with interleukin (IL)12, IL21, and CXCR3, or DNA-based vaccination followed by synthetic peptide-based booster immunization against tumor antigens Trp1, survivin, polo-like kinase-1 (PLK1). Moreover, Multi-antigen-specific antitumor immunity could be induced by using DNA encoding melanoma-specific antigenic epitopes Trp1455, Trp2180, and gp10025 linked to furin-sensitive linker RVKR. Likewise, the use of
antibodies stimulating costimulatory molecules OX40 and 4-1BB instead of anti-CD40 antibodies in peptide-vaccine mixtures results in potent anti-tumor immunity, and most of TLR-ligands poly-IC (TLR3-L), CpG (TLR9-L), Pam2CSk4 (TLR2-L), and Gardiquimod (GDQ; TLR7-L), [except LPS (TLR4-L)] were able to elicit antigen-specific CD8 T-cell responses.
Particularly, we have established mouse melanoma/leukemia/ hepatoma models close to clinical setting with luciferase- expressing tumor cell lines to monitor tumor growth with in vivo imaging methods. The improved antitumor effects of the DC-based/peptide-based vaccine strategy using zoledronate and rapamycin, which are used as anticancer drugs for osteoporosis and some hematological cancers, were examined in mouse orthotopic leukemia and solid tumors (melanoma/colorectal cancer) models. Furthermore, synergistic effects of anti-IL-2/IL2 complex and PD-1/PD-L1 blockade combined with zoledronate and the characteristics of antigen-specific T cells in tumor microenvironment were also investigated. T cells were transduced with the melanoma-specific antigen gp10025-targeting TCR gene and verified the antigen-targeting capabilities.
High-avidity antigen-specific CD8 T cells that recognize HLA-A2-positive human tumor cells were induced by a heterologous-vaccine strategy in HLA-A2 Tg mice, and HLA-A2-expressing tumor cell lines were established for the evaluation of anti-tumor effects of the heterologous-vaccine strategy in HLA-A2 Tg mouse-tumor models. The overall results suggest that combined immunological strategies allow the design of effective vaccination strategies against cancer, which may circumvent current limitations of cancer therapeutic vaccine that shows lsuboptimal therapeutic efficacies. Moreover, similar strategies would be applicable for the design of off-the-shelf therapeutic vaccines in antibody-based and/or adoptive immunotherapy for treating viral diseases and various cancers.
Expected Contribution
The optimization of heterogeous prime-boost vaccination allows the design of effective vaccination strategies against cancer, which may circumvent current limitations of DC-based vaccine that shows low immune responses and suboptimal therapeutic efficacies. Moreover, similar strategies would be applicable for the design of off-the-shelf therapeutic vaccines in cancer immunotherapy for treating viral diseases and various cancers, achieving desired clinical results in cancer patients.
(source : SUMMARY 13p)
 표
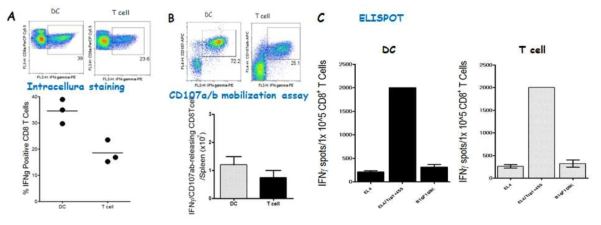
Comparison of CD8 T cell responses induced with TriVax booster immunization after priming with peptide-loaded DCs or T cells. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs or T cells (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 μg Trp1455/9M, 50 μg poly-IC, and 100 μg anti-CD40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
표
Comparison of CD8 T cell responses induced with TriVax booster immunization after priming with peptide-loaded DCs or T cells. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs or T cells (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 μg Trp1455/9M, 50 μg poly-IC, and 100 μg anti-CD40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
 표
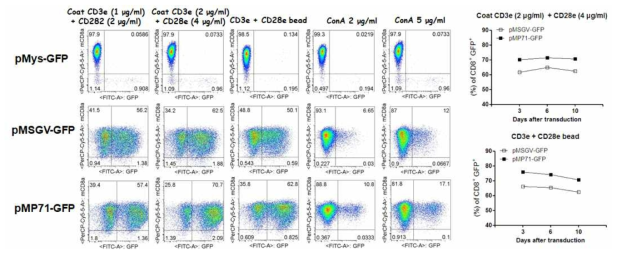
Expression of GFP on activated T cells in various conditions. Freshly isolated T cells from spleen using immunomagnetic beads were pre-activated with indicated conditions for 2 days. The ex vivo activated T cells were transduced with recombinant retroviruses encoding GFP, which were generated using pMys, pMSCV, and pMP71 vectors (pMys-GFP, pMSCV-GFP, and pMP71-GFP, respectively), followed by culturing in presence of 500U/ml IL-2. The expression of GFP on genetically modified T cells were chased for 10 days as indicated. The cells from each group were harvested and the expression of GFP analyzed by flow cytometry
표
Expression of GFP on activated T cells in various conditions. Freshly isolated T cells from spleen using immunomagnetic beads were pre-activated with indicated conditions for 2 days. The ex vivo activated T cells were transduced with recombinant retroviruses encoding GFP, which were generated using pMys, pMSCV, and pMP71 vectors (pMys-GFP, pMSCV-GFP, and pMP71-GFP, respectively), followed by culturing in presence of 500U/ml IL-2. The expression of GFP on genetically modified T cells were chased for 10 days as indicated. The cells from each group were harvested and the expression of GFP analyzed by flow cytometry
 표
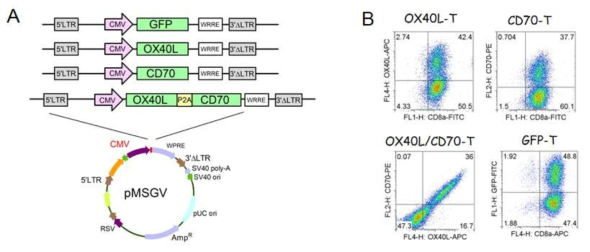
Expression of costimulatory ligands OX40L, CD70, and OX40L/CD70 on activated T-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse OX40L, CD70, and OX40L/CD70. The OX40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pMSGV retroviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated T-cells were transduced with recombinant retroviruses encoding GFP, OX40L, CD70, and OX40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
표
Expression of costimulatory ligands OX40L, CD70, and OX40L/CD70 on activated T-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse OX40L, CD70, and OX40L/CD70. The OX40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pMSGV retroviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated T-cells were transduced with recombinant retroviruses encoding GFP, OX40L, CD70, and OX40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
 표
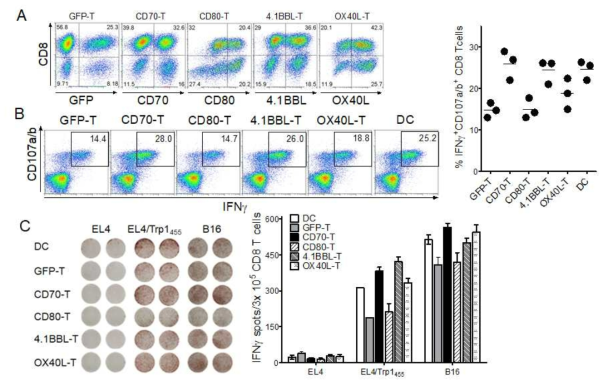
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with genetically modified T cells. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, CD80, 4-1BBL, and OX40L (GFP-T, CD70-T, CD80-T, 4-1BBL-T, and OX40L-T, respectively). B6 mice were immunized intravenously with either Trp1455-pulsed variously conditioned T cells (prime); 7 days later, the mice received a TriVax booster immunization. B. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ and CD107a/b staining after coculturing with Trp1455 peptide. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated for their capacity to recognize target cells using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
표
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with genetically modified T cells. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, CD80, 4-1BBL, and OX40L (GFP-T, CD70-T, CD80-T, 4-1BBL-T, and OX40L-T, respectively). B6 mice were immunized intravenously with either Trp1455-pulsed variously conditioned T cells (prime); 7 days later, the mice received a TriVax booster immunization. B. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ and CD107a/b staining after coculturing with Trp1455 peptide. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated for their capacity to recognize target cells using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
 표
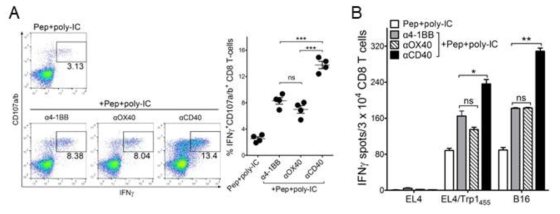
Peptide-based booster immunization after priming with CD70-T-cells drives enhanced CD8 T-cell responses. B6 mice (2 per group) were immunized intravenously on day 0 with 2 × 106 Trp1455/9M-loaded CD70-T-cells; 7-days later, the mice received a booster immunization with various combination of 100 μg of Trp1455/9M peptide, 50 μg of poly-IC, and 50 μg anti-CD40, anti-4-1BB, or anti-OX40Abs. A. 7-days after last immunization, the frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
표
Peptide-based booster immunization after priming with CD70-T-cells drives enhanced CD8 T-cell responses. B6 mice (2 per group) were immunized intravenously on day 0 with 2 × 106 Trp1455/9M-loaded CD70-T-cells; 7-days later, the mice received a booster immunization with various combination of 100 μg of Trp1455/9M peptide, 50 μg of poly-IC, and 50 μg anti-CD40, anti-4-1BB, or anti-OX40Abs. A. 7-days after last immunization, the frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
 표
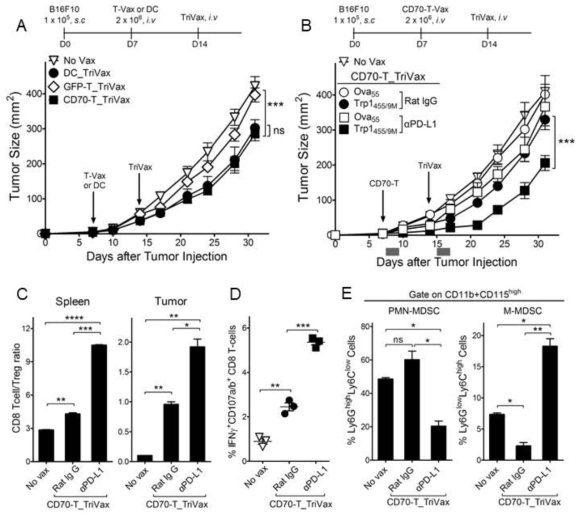
PD-L1 blockade augments the therapeutic efficacy of CD70-T_TriVax vaccination. A. Therapeutic efficacy of CD70-T_TriVax vaccination against advanced B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells, followed by vaccination with 2 × 106 GFP-T or CD70-T-cells on day 7, and TriVax on day 14. Non-vaccinated mice (No vax) and DC_TriVax were included for comparison. B. PD-L1 blockade enhanced the efficacy of CD70-T_TriVax vaccination regimen. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized as described above. Rat IgG (as controls) and anti-PD-L1 Abs were administered intraperitoneally on days +1 and +3 after each immunization. No vaccinated (No Vax) and Ova55-loaded CD70-T_TriVax vaccinated mice (Ova55) were included for comparison. C-E. In a parallel with B, mice were sacrificed on day 21, and the CD8 T-cell responses and immune cell populations were evaluated. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells per percentage of CD4+ Foxp3+T-cells in each group. D. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. E. Quantification of Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in tumor sites
표
PD-L1 blockade augments the therapeutic efficacy of CD70-T_TriVax vaccination. A. Therapeutic efficacy of CD70-T_TriVax vaccination against advanced B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells, followed by vaccination with 2 × 106 GFP-T or CD70-T-cells on day 7, and TriVax on day 14. Non-vaccinated mice (No vax) and DC_TriVax were included for comparison. B. PD-L1 blockade enhanced the efficacy of CD70-T_TriVax vaccination regimen. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized as described above. Rat IgG (as controls) and anti-PD-L1 Abs were administered intraperitoneally on days +1 and +3 after each immunization. No vaccinated (No Vax) and Ova55-loaded CD70-T_TriVax vaccinated mice (Ova55) were included for comparison. C-E. In a parallel with B, mice were sacrificed on day 21, and the CD8 T-cell responses and immune cell populations were evaluated. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells per percentage of CD4+ Foxp3+T-cells in each group. D. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. E. Quantification of Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in tumor sites
 표
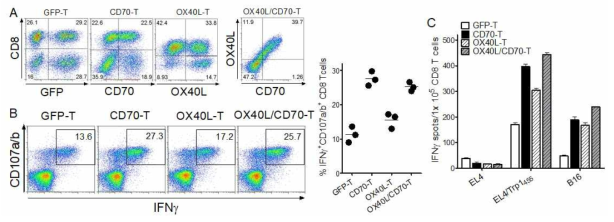
Evaluation of heterogenous vaccination regimen with genetically modified T cell co-expressing OX40L and CD70. A. T cells were transduced individually or together with recombinant retroviruses encoding GFP, CD70, and OX40L as indicated (GFP-T, CD70-T, OX40L-T, and OX40L/CD70-T, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
표
Evaluation of heterogenous vaccination regimen with genetically modified T cell co-expressing OX40L and CD70. A. T cells were transduced individually or together with recombinant retroviruses encoding GFP, CD70, and OX40L as indicated (GFP-T, CD70-T, OX40L-T, and OX40L/CD70-T, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
 표
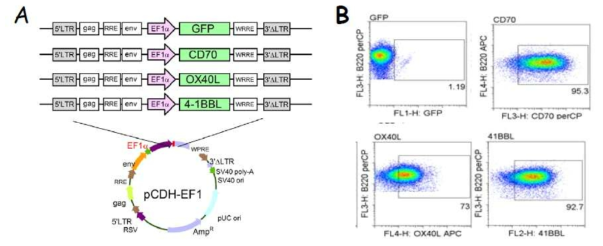
Expression of additional costimulatory ligands CD70, OX40L, and 4-1BBL on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD70, OX40L, and 4-1BBL. The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
표
Expression of additional costimulatory ligands CD70, OX40L, and 4-1BBL on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD70, OX40L, and 4-1BBL. The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
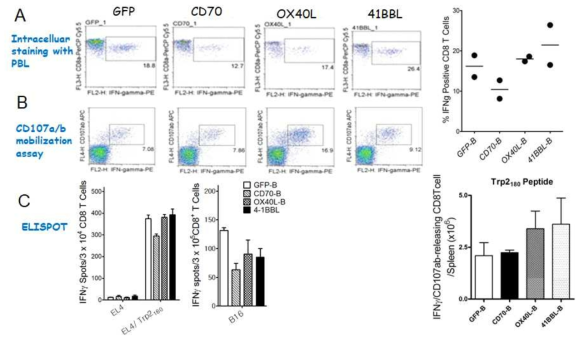 표
Induction of antigen-specific CD8 T cell responses using heterogenous immunization after priming with peptide-loaded B cells, which are transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually (GFP-B, CD70-B, Ox40L-B, and 4-1BBL-B, respectively). B6 mice were immunized intravenously with Trp2180-pulsed variously conditioned B cells (prime); 7 days later, the mice received a booster immunization with TriVax. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp2180 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma
표
Induction of antigen-specific CD8 T cell responses using heterogenous immunization after priming with peptide-loaded B cells, which are transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually (GFP-B, CD70-B, Ox40L-B, and 4-1BBL-B, respectively). B6 mice were immunized intravenously with Trp2180-pulsed variously conditioned B cells (prime); 7 days later, the mice received a booster immunization with TriVax. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp2180 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma
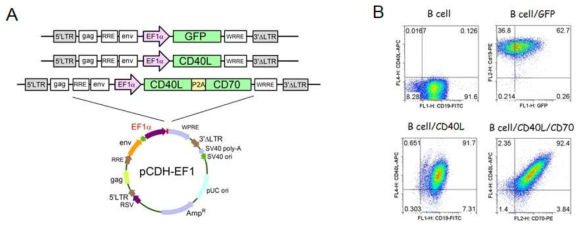 표
Expression of costimulatory ligands CD40L, and CD40L/CD70 on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD40L, and CD40L/CD70. The CD40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
표
Expression of costimulatory ligands CD40L, and CD40L/CD70 on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD40L, and CD40L/CD70. The CD40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
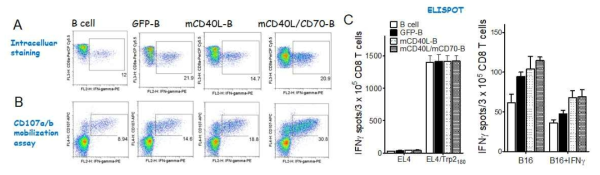 표
Evaluation of heterogenous vaccination regimen with genetically modified B cell co-expressing CD40L and CD70. A. T cells were transduced individually or together with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70 (GFP-B, CD40L-B, and CD40L/CD70-B, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 7 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
표
Evaluation of heterogenous vaccination regimen with genetically modified B cell co-expressing CD40L and CD70. A. T cells were transduced individually or together with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70 (GFP-B, CD40L-B, and CD40L/CD70-B, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 7 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
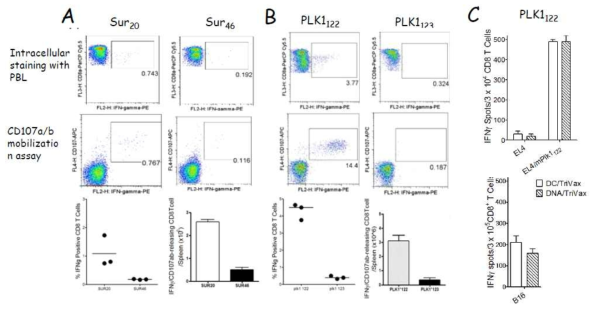 표
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with DNA plasmid constructs encoding Survivin (A) or polo-like kinase (PLK1; B). Mice (3 per group) were vaccinated intramuscularly. with DNA plasmid followed immediately by electroporation of the injected area (95 V, 4 X 65 ms pulses with repoling) using TX830 Electro Square Porator device. 14 days later, the mice received a booster immunization with TriVax composed of 100 mg of peptide (as indicated), 50mg of poly-IC, and 100 mg of anti-CD40. 7 days later after last immunization, blood sample were evaluated by intracellular IFNγ staining, and total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. CD8 T cells were purified from pooled splenocytes of mice primed differently either peptide-loaded DC or DNA plasmids, and antigen-induced IFNγ secretion to PLK1122 (DSDFVFVVL) peptide was evaluated in EliSpot assays using peptide-pulsed APCs and B16 melanoma
표
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with DNA plasmid constructs encoding Survivin (A) or polo-like kinase (PLK1; B). Mice (3 per group) were vaccinated intramuscularly. with DNA plasmid followed immediately by electroporation of the injected area (95 V, 4 X 65 ms pulses with repoling) using TX830 Electro Square Porator device. 14 days later, the mice received a booster immunization with TriVax composed of 100 mg of peptide (as indicated), 50mg of poly-IC, and 100 mg of anti-CD40. 7 days later after last immunization, blood sample were evaluated by intracellular IFNγ staining, and total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. CD8 T cells were purified from pooled splenocytes of mice primed differently either peptide-loaded DC or DNA plasmids, and antigen-induced IFNγ secretion to PLK1122 (DSDFVFVVL) peptide was evaluated in EliSpot assays using peptide-pulsed APCs and B16 melanoma
 표
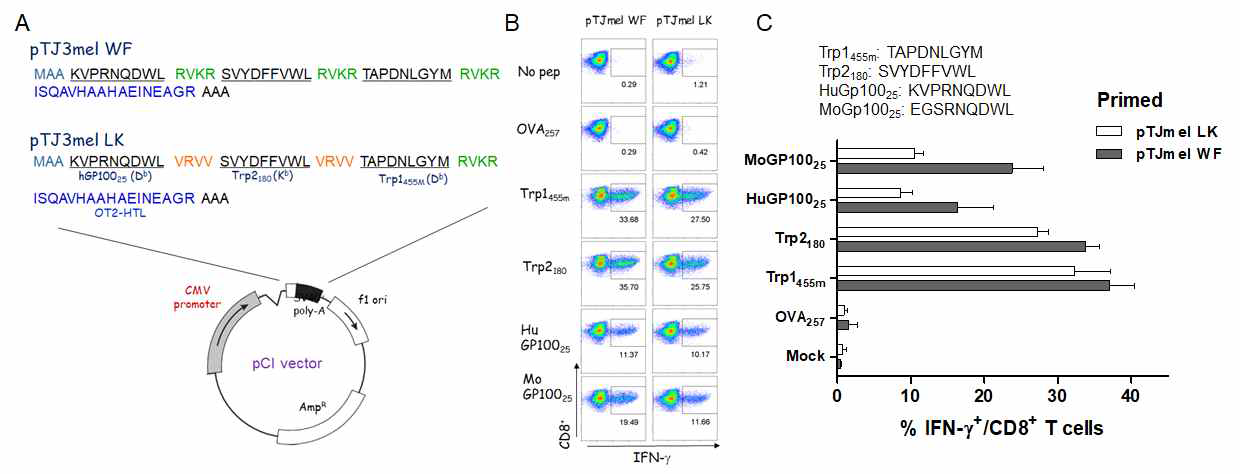
Mul-ti-epitope-coding DNA priming followed by TriVax boost with multi-peptides induces concurrent CD8 T cell responses. A. Multi-epitope plasmid constructs coding three CD8 T cell epitopes for melanosomal antigens and a CD4 T cell epitope OT2 linked with furin-sensitive (RVKR) or furin-insensitive spacer (VRVV). B and C. Induction of antigen-specific CD8 T cell responses using DNA plasmid encoding multi-epitopes drived from melanosomal antigens. Anesthetized mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830 device. 14 days later, the mice were received booster immunization. B. 8 days after the boost, the presence of antigen-specific CD8 T cell responses in spleen were evaluated by intracellular IFNγ staining after coculturing with individual peptides (Ova257, Trp1455, Trp2180, Hugp10025, and Mogp10025). C. Freshly isolated CD8 T ells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, and EL4/mgp10025, respectively), and un-pulsed EL4
표
Mul-ti-epitope-coding DNA priming followed by TriVax boost with multi-peptides induces concurrent CD8 T cell responses. A. Multi-epitope plasmid constructs coding three CD8 T cell epitopes for melanosomal antigens and a CD4 T cell epitope OT2 linked with furin-sensitive (RVKR) or furin-insensitive spacer (VRVV). B and C. Induction of antigen-specific CD8 T cell responses using DNA plasmid encoding multi-epitopes drived from melanosomal antigens. Anesthetized mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830 device. 14 days later, the mice were received booster immunization. B. 8 days after the boost, the presence of antigen-specific CD8 T cell responses in spleen were evaluated by intracellular IFNγ staining after coculturing with individual peptides (Ova257, Trp1455, Trp2180, Hugp10025, and Mogp10025). C. Freshly isolated CD8 T ells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, and EL4/mgp10025, respectively), and un-pulsed EL4
 표
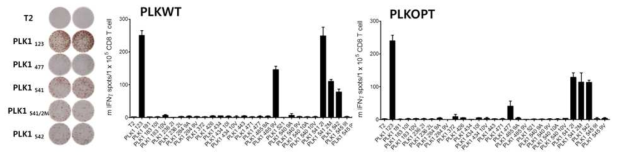
Induction of antigen-specific CD8 T cell responses on HLA-A2 transgeneic mice using synthetic DNA plasmid encoding putative HLA-A2-restricted multi-epitopes drived from human PLK1. Mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA, injected three times at interval of 7 days, followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830. 8 days after the last immunization, the presence of antigen-specific CD8 T cell responses in spleen were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 as indicated, and un-pulsed EL4 cells (negative control)
표
Induction of antigen-specific CD8 T cell responses on HLA-A2 transgeneic mice using synthetic DNA plasmid encoding putative HLA-A2-restricted multi-epitopes drived from human PLK1. Mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA, injected three times at interval of 7 days, followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830. 8 days after the last immunization, the presence of antigen-specific CD8 T cell responses in spleen were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 as indicated, and un-pulsed EL4 cells (negative control)
 표
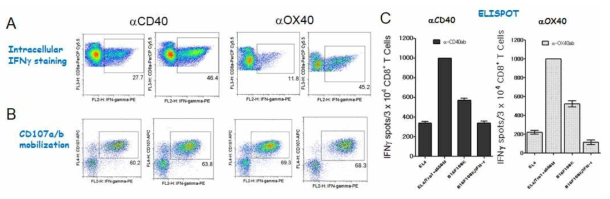
Comparison of CD8 T cell responses induced with TriVax booster immunization, which are composed with anti-CD40 or anti-OX40 in DC-prime/TriVax-boost vaccination regime. B6 mice (2 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs; 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 50mg of poly-IC, and 100 mg of either anti-CD40 or anti-Ox40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells from pooled splenocytes was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
표
Comparison of CD8 T cell responses induced with TriVax booster immunization, which are composed with anti-CD40 or anti-OX40 in DC-prime/TriVax-boost vaccination regime. B6 mice (2 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs; 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 50mg of poly-IC, and 100 mg of either anti-CD40 or anti-Ox40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells from pooled splenocytes was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
 표
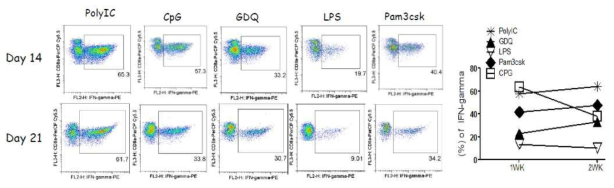
Effect of TLR-Ls on heterogenous peptide-loaded DC prime/TriVax boost regime. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 100 mg of anti-CD40, and one of the following TLR-L: Poly-IC (TLR3-L), CpG (TLR9-L), LPS (TLR4-L), Pam2CSk4 (TLR2-L), and GDQ (TLR7-L). The frequency of Trp1455-specific CD8 T cells in peripheral blood was evaluated by intracellular IFNγ staining in individual mice for 2 weeks (on day 14 and 21)
표
Effect of TLR-Ls on heterogenous peptide-loaded DC prime/TriVax boost regime. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 100 mg of anti-CD40, and one of the following TLR-L: Poly-IC (TLR3-L), CpG (TLR9-L), LPS (TLR4-L), Pam2CSk4 (TLR2-L), and GDQ (TLR7-L). The frequency of Trp1455-specific CD8 T cells in peripheral blood was evaluated by intracellular IFNγ staining in individual mice for 2 weeks (on day 14 and 21)
 표
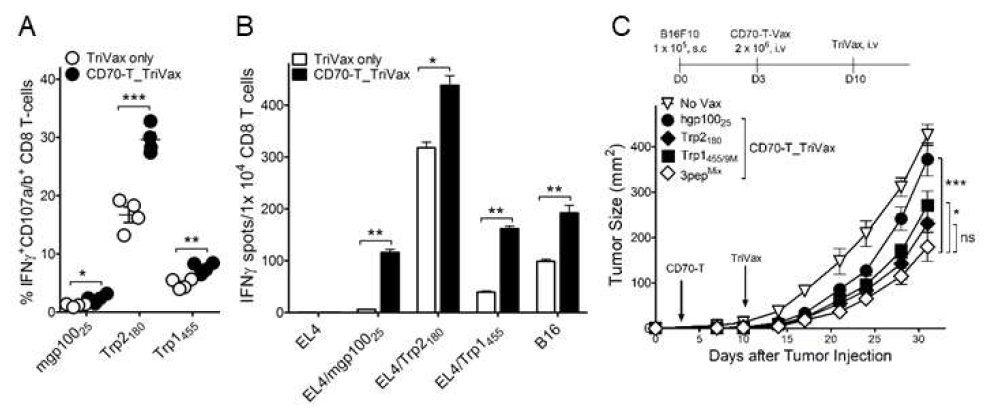
Multi-epitope-loaded CD70-T-cells priming followed by TriVax booster immunization induces concurrent effective antitumor CD8 T cell responses. B6 mice were immunized intravenously with CD70-T-cells that were loaded with mixture of Trp1455/9M, Trp2180, and hgp10025 peptides; 7-days later, the mice received 3pepMIXTriVax. A. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455, Trp2180, mgp10025-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, EL4/mgp10025), B16 melanoma. C. Therapeutic effectiveness of multi-epitope-loaded CD70-T_TriVax immunization against 3-day-established B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized intravenously on day 3, and 10 in combination with CD70-T or TriVax using either individual peptide or mixture of Trp1455/9M, Trp2180, and hgp10025 (3pepMIX) peptides as indicated
표
Multi-epitope-loaded CD70-T-cells priming followed by TriVax booster immunization induces concurrent effective antitumor CD8 T cell responses. B6 mice were immunized intravenously with CD70-T-cells that were loaded with mixture of Trp1455/9M, Trp2180, and hgp10025 peptides; 7-days later, the mice received 3pepMIXTriVax. A. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455, Trp2180, mgp10025-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, EL4/mgp10025), B16 melanoma. C. Therapeutic effectiveness of multi-epitope-loaded CD70-T_TriVax immunization against 3-day-established B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized intravenously on day 3, and 10 in combination with CD70-T or TriVax using either individual peptide or mixture of Trp1455/9M, Trp2180, and hgp10025 (3pepMIX) peptides as indicated
 표
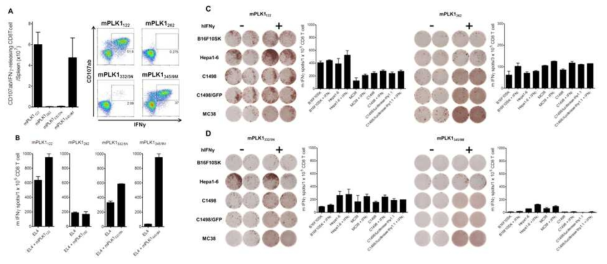
Induction of PLK1–specific CD8 T cell responses using DCs prime/TriVax immunization regimen in C57BL/6j mice. Mice were vaccinated i.v. on day 0 with DCs loaded with each peptide, mPLK1122 (DSDFVFVVL), mPLK1262 (RIKKNEYSI), mPLK1332 (LDPSSRKPL), mPLK1345 (KGVENPLPD) for priming. 7 days later, the mice were received booster immunizatin with TriVax composed 150 μg of peptide, 50 μg of poly-IC, and 100 μg of anti-CD40. A. Eight days after the boost, splenocytes from each individual mouse were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells (B), B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells (C-D) as indicated. Un-pulsed EL4 cells were used as controls
표
Induction of PLK1–specific CD8 T cell responses using DCs prime/TriVax immunization regimen in C57BL/6j mice. Mice were vaccinated i.v. on day 0 with DCs loaded with each peptide, mPLK1122 (DSDFVFVVL), mPLK1262 (RIKKNEYSI), mPLK1332 (LDPSSRKPL), mPLK1345 (KGVENPLPD) for priming. 7 days later, the mice were received booster immunizatin with TriVax composed 150 μg of peptide, 50 μg of poly-IC, and 100 μg of anti-CD40. A. Eight days after the boost, splenocytes from each individual mouse were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells (B), B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells (C-D) as indicated. Un-pulsed EL4 cells were used as controls
 표
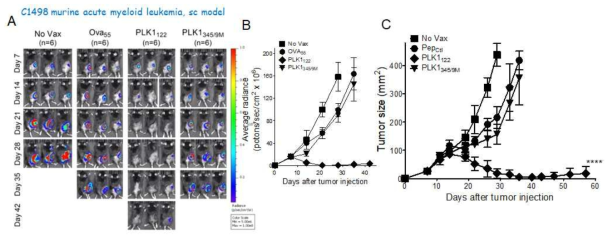
DC-prime/TriVax vaccination with mPLK1122 epitopes results in strong antitumor effects against established C1498 leukemia. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122 or mPLK1345/9M-vaccinated group
표
DC-prime/TriVax vaccination with mPLK1122 epitopes results in strong antitumor effects against established C1498 leukemia. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122 or mPLK1345/9M-vaccinated group
 표
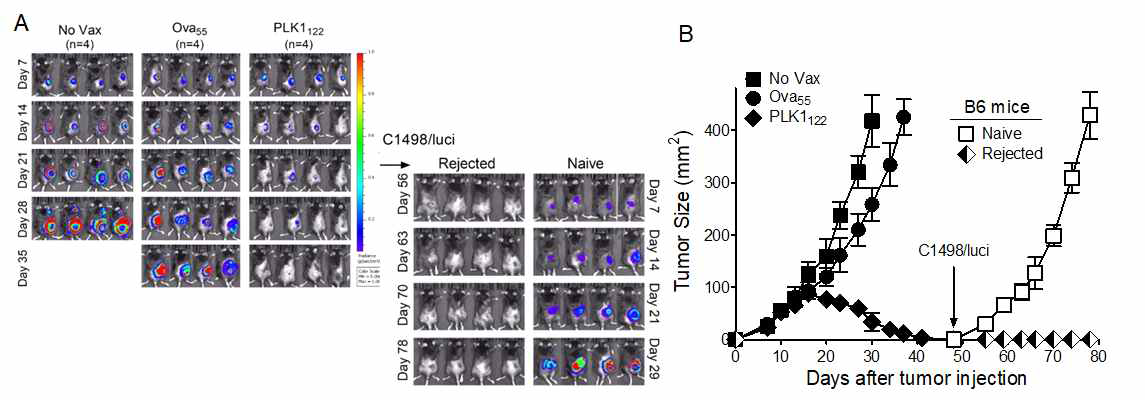
Memory antitumor effects of DC-prime/TriVax vaccination with mPLK1122 epitopes. A. At the termination of the experiment presented in Fig. 16, tumor-free (rejected) B6 mice (4 per group) received subcutaneous tumor rechallenge with 2 x 106 live luciferase-expressing C1498 (C1498/Luci) cells (in the opposite flank). Naïve, unvaccinated mice inoculated with the same number of C1498/Luci cells were included as controls
표
Memory antitumor effects of DC-prime/TriVax vaccination with mPLK1122 epitopes. A. At the termination of the experiment presented in Fig. 16, tumor-free (rejected) B6 mice (4 per group) received subcutaneous tumor rechallenge with 2 x 106 live luciferase-expressing C1498 (C1498/Luci) cells (in the opposite flank). Naïve, unvaccinated mice inoculated with the same number of C1498/Luci cells were included as controls
 표
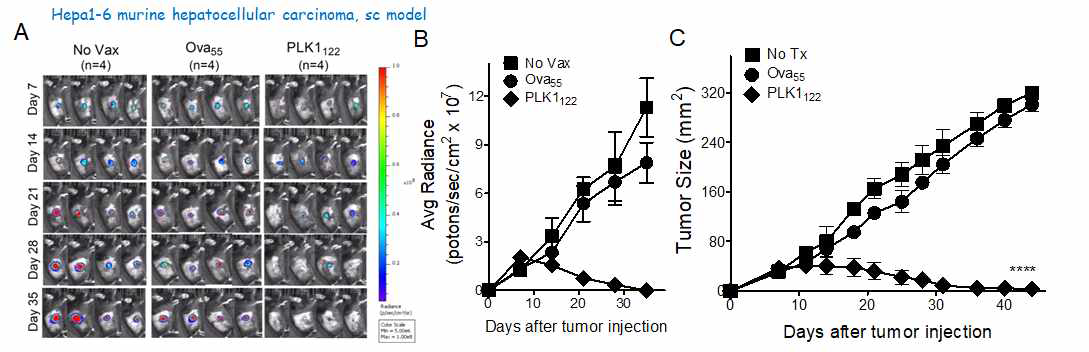
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established Hepa1-6 hepatocacinoma. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing Hepa1-6 cells, and vaccinated intravenously as in Fig. 16. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122-vaccinated group
표
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established Hepa1-6 hepatocacinoma. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing Hepa1-6 cells, and vaccinated intravenously as in Fig. 16. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122-vaccinated group
 표
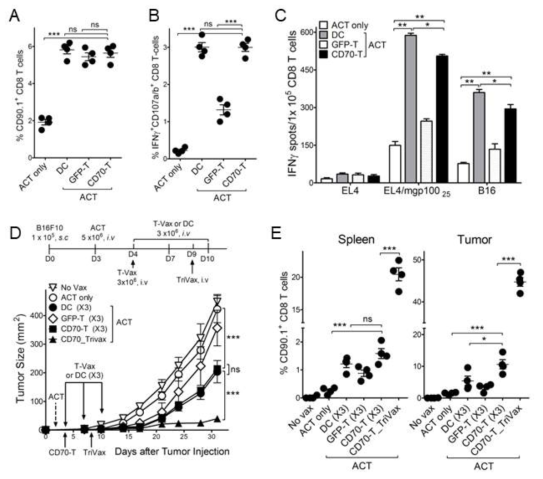
Effects of CD70-T vaccination in antitumor efficacy of adoptive T-cell therapy. A-C. B6 mice were adoptively transferred 5 × 106 naive Pmel-1 T-cells on day 0, followed by immunization on day 1 with 3 × 106 hgp10025-pulsed GFP-T and CD70-T-cells. Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. A. 7-days after the immunization, in vivo expansion of Pmel-1 T-cells (CD90.1+ CD8 T-cells) in spleen was assessed. B. The frequency of mgp10025-specific CD8 T-cells was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. C. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes were evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: mgp10025-pulsed EL4 (EL4/mgp10025), B16 melanoma. D. Antitumor effects of CD70-T immunization after pmel-1 ACT. B6 mice (5 per group) were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and received 5 × 106 Pmel-1 cells on day 3 followed by vaccination with hgp10025-pulsed GFP-T and CD70-T-cells thrice (on day 4, 7, and 10: D, vertical arrows). For CD70-T_TriVax regimen, TriVax was administered intravenously 5-days after CD70-T vaccination. Non-vaccinated mice (No Vax), Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. E. In a parallel with D , respectively, mice (4 per group) were sacrificed on day 21, and the frequency of Pmel-1 T-cells in spleen and tumor site was evaluated
표
Effects of CD70-T vaccination in antitumor efficacy of adoptive T-cell therapy. A-C. B6 mice were adoptively transferred 5 × 106 naive Pmel-1 T-cells on day 0, followed by immunization on day 1 with 3 × 106 hgp10025-pulsed GFP-T and CD70-T-cells. Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. A. 7-days after the immunization, in vivo expansion of Pmel-1 T-cells (CD90.1+ CD8 T-cells) in spleen was assessed. B. The frequency of mgp10025-specific CD8 T-cells was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. C. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes were evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: mgp10025-pulsed EL4 (EL4/mgp10025), B16 melanoma. D. Antitumor effects of CD70-T immunization after pmel-1 ACT. B6 mice (5 per group) were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and received 5 × 106 Pmel-1 cells on day 3 followed by vaccination with hgp10025-pulsed GFP-T and CD70-T-cells thrice (on day 4, 7, and 10: D, vertical arrows). For CD70-T_TriVax regimen, TriVax was administered intravenously 5-days after CD70-T vaccination. Non-vaccinated mice (No Vax), Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. E. In a parallel with D , respectively, mice (4 per group) were sacrificed on day 21, and the frequency of Pmel-1 T-cells in spleen and tumor site was evaluated
 표
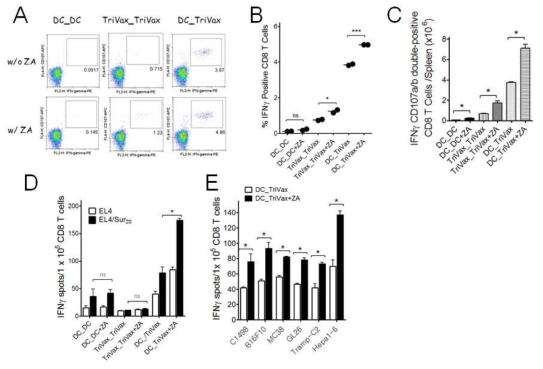
Combination of zoledonate on peptide-loaded DC-prime/TriVax booster immunization elicits enhanced CD8 T cell responses. B6 mice were immunized intravenously with Sur20 (ATFKNWPFL)-pulsed DC or TriVax; 7 days later, the mice received a combinatorial booster immunization. Zoledonate was administered on day 1 and 3 after vaccination. A and B. 8 days after the boost, the presence of Trp1455-specific CD8 T cells in spleen was evaluated by intracellular IFNγ staining after coculturing with Sur20 peptide. C. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. D and E. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Sur20), C1498 acute myeloid leukemia, B16 melanoma, MC38 colon adenocarcinoma, GL26 glioblastoma, Tramp-C2, prostate adenocarcinoma, and Hepa1-6 hepatoma
표
Combination of zoledonate on peptide-loaded DC-prime/TriVax booster immunization elicits enhanced CD8 T cell responses. B6 mice were immunized intravenously with Sur20 (ATFKNWPFL)-pulsed DC or TriVax; 7 days later, the mice received a combinatorial booster immunization. Zoledonate was administered on day 1 and 3 after vaccination. A and B. 8 days after the boost, the presence of Trp1455-specific CD8 T cells in spleen was evaluated by intracellular IFNγ staining after coculturing with Sur20 peptide. C. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. D and E. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Sur20), C1498 acute myeloid leukemia, B16 melanoma, MC38 colon adenocarcinoma, GL26 glioblastoma, Tramp-C2, prostate adenocarcinoma, and Hepa1-6 hepatoma
 표
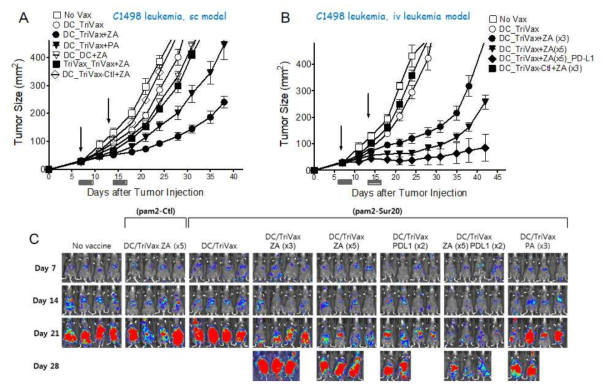
Combined effects of zoledonate (ZA) on therapeutic immunity in DC prime-TriVax boost vaccination strategy against established C1498 leukemia. A and B. B6 mice (4 per group) were inoculated subcutaneously on day 0 with 3 X 105 C1498 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, Pamidronate (PA), and anti-PD-L1 was administered on day 1 and 3 after vaccination. A. Effects of ZA in combinatorial vaccination on the therapeutic efficacy of antigen-loaded DCs and TriVax immunization. B and C. For leukemic tumor model, B6 mice were infused intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated on day 7 and 14. Time course of bioluminescence in individual mice from both treatment groups
표
Combined effects of zoledonate (ZA) on therapeutic immunity in DC prime-TriVax boost vaccination strategy against established C1498 leukemia. A and B. B6 mice (4 per group) were inoculated subcutaneously on day 0 with 3 X 105 C1498 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, Pamidronate (PA), and anti-PD-L1 was administered on day 1 and 3 after vaccination. A. Effects of ZA in combinatorial vaccination on the therapeutic efficacy of antigen-loaded DCs and TriVax immunization. B and C. For leukemic tumor model, B6 mice were infused intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated on day 7 and 14. Time course of bioluminescence in individual mice from both treatment groups
 표
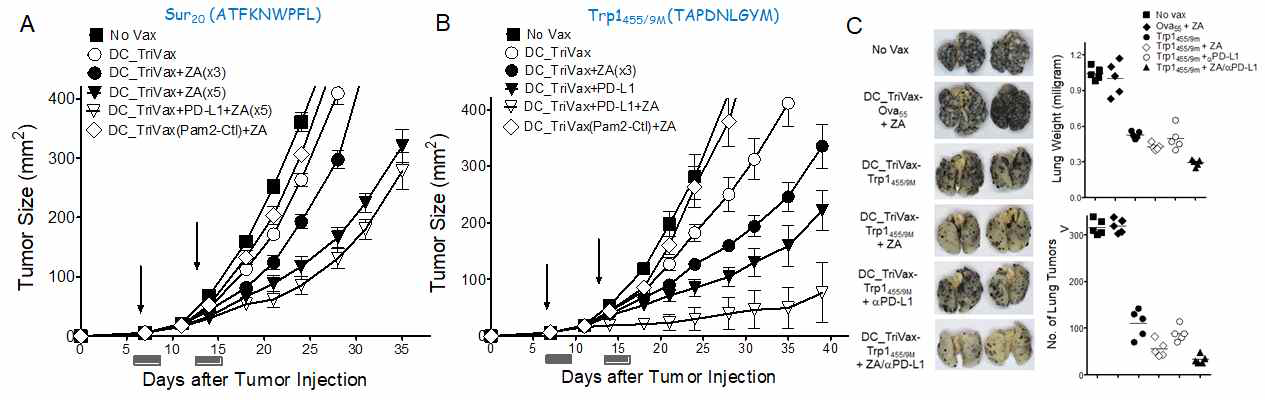
Zoledronate and PD1 blockade revealed synergic therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established B16 melanoma. A and B. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated using either Sur20 (ATFKNWPFL: A) or Trp1455/9M (TAPDNLGYM: B). ZA and anti-PD-L1 was administered on day 1 and 3 after vaccination. C. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
표
Zoledronate and PD1 blockade revealed synergic therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established B16 melanoma. A and B. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated using either Sur20 (ATFKNWPFL: A) or Trp1455/9M (TAPDNLGYM: B). ZA and anti-PD-L1 was administered on day 1 and 3 after vaccination. C. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
 표
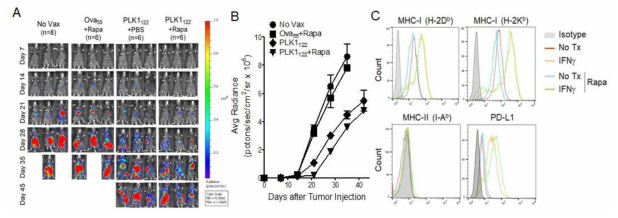
Rapamycin enhance the therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14. Rapamycin wwas administered intraperitoneally (1 mg/kg) for three days after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry
표
Rapamycin enhance the therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14. Rapamycin wwas administered intraperitoneally (1 mg/kg) for three days after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry
 표
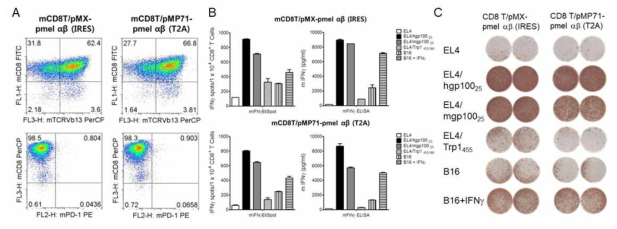
Expression and biological function of TCR-engineered T cells transduced with gp10025-specific (pmel) mTCR, which was cloned together with IRES or T2A linker. A. Flow cytometric analysis of gp10025-specific mTCR-transduced mouse T cells. B-C. The antigen-specificity of pmel TCR-engineered T cells was evaluated by IFNγ EliSpot or ELISA assay with peptide-pulsed EL4 cells, B16 melanoma as indicated. The peptides gp10025 (KVPRNQDWL), mgp10025 (EGSRNQDWL), or Trp1455 (TAPDNLGYA) were used for pulsing on EL4 cells. Un-pulsed EL4 cells were used as controls
표
Expression and biological function of TCR-engineered T cells transduced with gp10025-specific (pmel) mTCR, which was cloned together with IRES or T2A linker. A. Flow cytometric analysis of gp10025-specific mTCR-transduced mouse T cells. B-C. The antigen-specificity of pmel TCR-engineered T cells was evaluated by IFNγ EliSpot or ELISA assay with peptide-pulsed EL4 cells, B16 melanoma as indicated. The peptides gp10025 (KVPRNQDWL), mgp10025 (EGSRNQDWL), or Trp1455 (TAPDNLGYA) were used for pulsing on EL4 cells. Un-pulsed EL4 cells were used as controls
 표
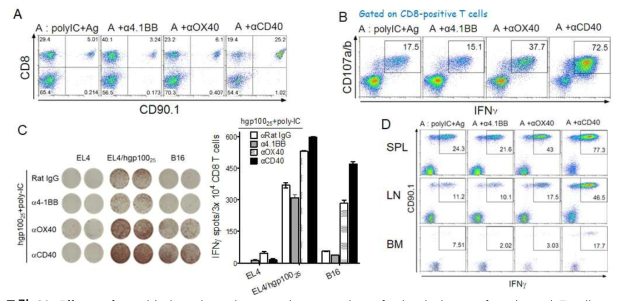
Effects of peptide-based vaccines on the expansion of adoptively transferred pmel T cells. B6 mice were adoptively transferred with 2 ⨯ 106 naive Pmel T cells followed by immunization one day later with various combinations of 100 mg of hgp10025 peptide, 50 mg of poly-IC, 100 mg of anti-CD40, anti-4.1BB, and anti-OX40 Abs as indicated. Eight days later, splenocytes from each mouse were examined for the expansion of pmel T cells (A), and antigen-specific recognition by intracellular IFNγ staining after coculturing with hgp10025 peptide (B) and EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma as indicated (C). D. Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
표
Effects of peptide-based vaccines on the expansion of adoptively transferred pmel T cells. B6 mice were adoptively transferred with 2 ⨯ 106 naive Pmel T cells followed by immunization one day later with various combinations of 100 mg of hgp10025 peptide, 50 mg of poly-IC, 100 mg of anti-CD40, anti-4.1BB, and anti-OX40 Abs as indicated. Eight days later, splenocytes from each mouse were examined for the expansion of pmel T cells (A), and antigen-specific recognition by intracellular IFNγ staining after coculturing with hgp10025 peptide (B) and EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma as indicated (C). D. Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
 표
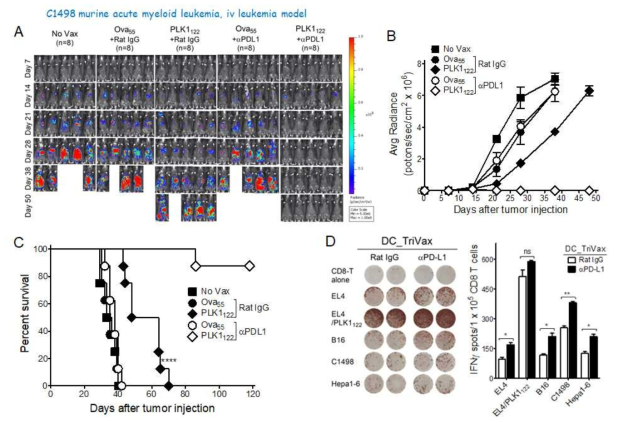
Heterologous vaccination with mPLK1122-DC-prime/TriVax prolongs survival of mice with C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. For PD-1 blockade, anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Kaplan–Mayer survival curves for all groups of mice. D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells as indicated. Un-pulsed EL4 cells were used as controls
표
Heterologous vaccination with mPLK1122-DC-prime/TriVax prolongs survival of mice with C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. For PD-1 blockade, anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Kaplan–Mayer survival curves for all groups of mice. D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells as indicated. Un-pulsed EL4 cells were used as controls
 표
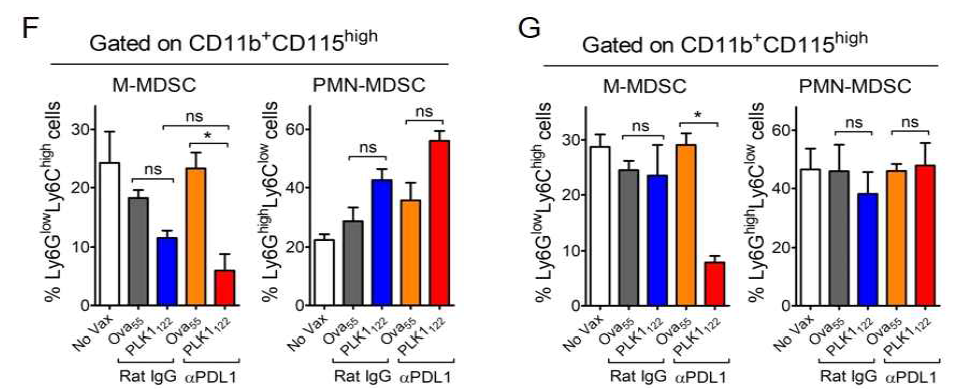
Effects of PD-L1 blockade on the therapeutic efficacy of PLK1122 DC_TriVax vaccination. In a parallel with Figure 1A, mice (3 per group) were sacrificed on day23, and the tissues and cells from disaggregated tissues were evaluated for the antitumor CD8 T-cell responses and immune cell populations. A. Frequency of PLK1122-specific CD8 T-cells in spleen was evaluated by intracellular IFNγ staining. Points, value for each individual mouse; horizontal line, average of the group. B. Freshly isolated CD8 T-cells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions by EliSpot against indicated target cells. Results represent the average number of spots from triplicate wells with SD (bars) of the means. C-G. Cells from disaggregated tissues of liver, bone-marrow (BM), spleen, and lung were analyzed by flow cytometry for the composition of tumor cells and various subsets of immune cells. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells/ percentage of CD4+ Foxp3+T-cells. D. Infiltration of (CD90.1-positive) C1498 leukemic cells. E. Representative flow cytometric plots showing Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in liver tissue. Results represent the average percentage of the gated cells from individual mice with SD (bars) of the means. P values were calculated using unpaired Student's t tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). These experiments were repeated twice with similar results
표
Effects of PD-L1 blockade on the therapeutic efficacy of PLK1122 DC_TriVax vaccination. In a parallel with Figure 1A, mice (3 per group) were sacrificed on day23, and the tissues and cells from disaggregated tissues were evaluated for the antitumor CD8 T-cell responses and immune cell populations. A. Frequency of PLK1122-specific CD8 T-cells in spleen was evaluated by intracellular IFNγ staining. Points, value for each individual mouse; horizontal line, average of the group. B. Freshly isolated CD8 T-cells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions by EliSpot against indicated target cells. Results represent the average number of spots from triplicate wells with SD (bars) of the means. C-G. Cells from disaggregated tissues of liver, bone-marrow (BM), spleen, and lung were analyzed by flow cytometry for the composition of tumor cells and various subsets of immune cells. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells/ percentage of CD4+ Foxp3+T-cells. D. Infiltration of (CD90.1-positive) C1498 leukemic cells. E. Representative flow cytometric plots showing Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in liver tissue. Results represent the average percentage of the gated cells from individual mice with SD (bars) of the means. P values were calculated using unpaired Student's t tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). These experiments were repeated twice with similar results
 표
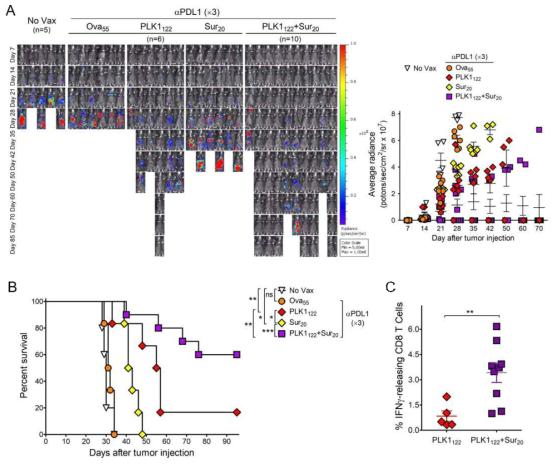
DCs priming followed by TriVax boost with multi-peptides with sustained PD-L1 blockade elicits augmented therapeutic effectiveness overcoming clonal heterogeneity of C1498 leukemia. B6 mice (6 to 10 per group) were intravenously 2×106 C1498-luc cells, and received DC_TriVax immunization using either individual peptide or mixture of PLK1122 and Sur20 (as indicated) with prolonged period of PD-L1 blockade, followed by weekly bioluminescence imaging. Non-vaccinated mice (No Vax) and Ova55DC_TriVax-vaccinated mice (Ova55) were included as controls. Anti-PD-L1 was administered three-times (x3) on days +1, +3 and +5 for long-term treatment after each immunization. A. Tumor growth was monitored by time course of in vivo bioluminescence imaging in individual mice (left panel), and average radiance per mouse is shown (right panel). Images were adjusted to the same pseudo color scale to show relative bioluminescence changes over time. Points, average values of photons in mouse; bars, SD. B. Kaplan-Mayer survival curves for all groups of mice in A. P values were determined by log-rank tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). C. Frequency of PLK1122-specific CD8T-cellswasevaluatedbyintracellularIFNg staining on day45 using blood samples from mice in A. Points, value for each individual mouse; horizontal line, average of the group. P values were calculated using unpaired Student’s t test (***, P <0.01). These experiments were repeated twice with similar results
표
DCs priming followed by TriVax boost with multi-peptides with sustained PD-L1 blockade elicits augmented therapeutic effectiveness overcoming clonal heterogeneity of C1498 leukemia. B6 mice (6 to 10 per group) were intravenously 2×106 C1498-luc cells, and received DC_TriVax immunization using either individual peptide or mixture of PLK1122 and Sur20 (as indicated) with prolonged period of PD-L1 blockade, followed by weekly bioluminescence imaging. Non-vaccinated mice (No Vax) and Ova55DC_TriVax-vaccinated mice (Ova55) were included as controls. Anti-PD-L1 was administered three-times (x3) on days +1, +3 and +5 for long-term treatment after each immunization. A. Tumor growth was monitored by time course of in vivo bioluminescence imaging in individual mice (left panel), and average radiance per mouse is shown (right panel). Images were adjusted to the same pseudo color scale to show relative bioluminescence changes over time. Points, average values of photons in mouse; bars, SD. B. Kaplan-Mayer survival curves for all groups of mice in A. P values were determined by log-rank tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). C. Frequency of PLK1122-specific CD8T-cellswasevaluatedbyintracellularIFNg staining on day45 using blood samples from mice in A. Points, value for each individual mouse; horizontal line, average of the group. P values were calculated using unpaired Student’s t test (***, P <0.01). These experiments were repeated twice with similar results
 표
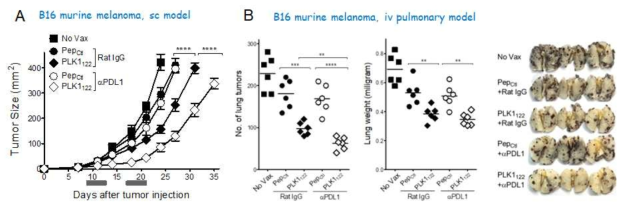
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established B16 melanoma. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 and anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after vaccination. B. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
표
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established B16 melanoma. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 and anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after vaccination. B. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
 표
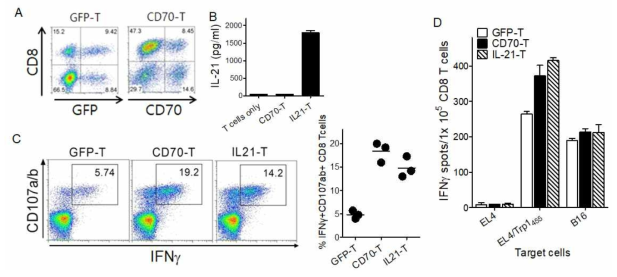
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing IL21. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, and IL21 as indicated (GFP-T, CD70-T, and IL21-T, respectively). B. The secretion of IL21 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (C and D)
표
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing IL21. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, and IL21 as indicated (GFP-T, CD70-T, and IL21-T, respectively). B. The secretion of IL21 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (C and D)
 표
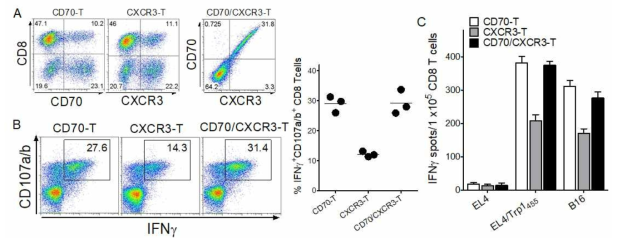
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing CD70 and CXCR3. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70 and CXCR3 as indicated (CD70-T, CXCR3-T and CD70/CXCR3-T, respectively). B and C. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
표
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing CD70 and CXCR3. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70 and CXCR3 as indicated (CD70-T, CXCR3-T and CD70/CXCR3-T, respectively). B and C. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
 표
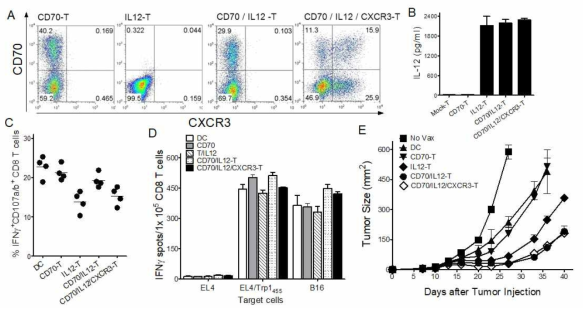
IL12-transduced T cells enhance the therapeutic efficacy of heterogenous vaccination regimen against established B16 melanoma. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70, IL12, and CXCR3 as indicated (CD70-T, IL12-T, CD70/IL12-T, and CD70/IL12/CXCR3-T, respectively). B. The secretion of IL12 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells, and B16 melanoma (C and D). For the therapeutic efficacy, B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 according to heterogenous vaccination regimen
표
IL12-transduced T cells enhance the therapeutic efficacy of heterogenous vaccination regimen against established B16 melanoma. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70, IL12, and CXCR3 as indicated (CD70-T, IL12-T, CD70/IL12-T, and CD70/IL12/CXCR3-T, respectively). B. The secretion of IL12 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells, and B16 melanoma (C and D). For the therapeutic efficacy, B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 according to heterogenous vaccination regimen
 표
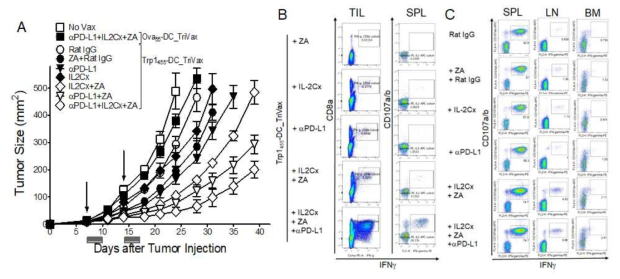
Zoledronate, PD-1 blockade and IL2Cx enhance the therapeutic efficacy of DCs prime-TriVax boost heterogenous vaccination regimen. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. Non-vaccinated mice (No Vax) and Ova55-loaded DCs prime-Ova55TriVax booster-vaccinated mice were included as controls. B. On day 24, the presence of peptide-specific CD8 T cells in tumor-infiltrating lymphocytes (TIL) and splenocytes (SPL) were evaluated by intracellular IFNγ and CD107a/b staining. C. B6 mice were immunized intravenously with Trp1455-pulsed DC (prime); 7 days later, the mice received a TriVax booster immunization and ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. On day 18 (post-boost), Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
표
Zoledronate, PD-1 blockade and IL2Cx enhance the therapeutic efficacy of DCs prime-TriVax boost heterogenous vaccination regimen. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. Non-vaccinated mice (No Vax) and Ova55-loaded DCs prime-Ova55TriVax booster-vaccinated mice were included as controls. B. On day 24, the presence of peptide-specific CD8 T cells in tumor-infiltrating lymphocytes (TIL) and splenocytes (SPL) were evaluated by intracellular IFNγ and CD107a/b staining. C. B6 mice were immunized intravenously with Trp1455-pulsed DC (prime); 7 days later, the mice received a TriVax booster immunization and ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. On day 18 (post-boost), Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
 표
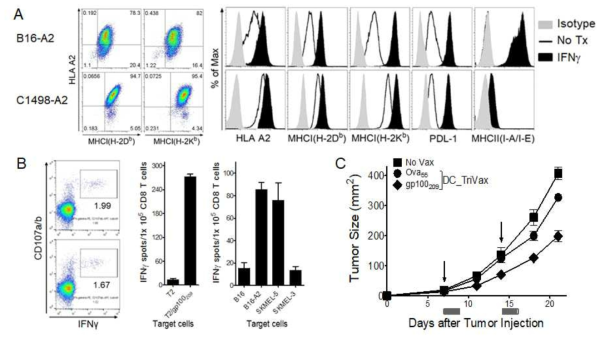
Establishment of HLA-A2-expressing mouse B16 (B16-A2) and C1498 (C1498-A2) cell lines. A. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry. B. HLA-A2 transgenic mice were immunized intravenously with gp100209 (ITDQVPFSV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. B. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining, and IFN-γ EliSpot assay against peptide-pulsed T2 (T2/gp100209), un-pulsed T2 cells, B16-A2, HLA-A2-positive human melanoma SKMEL-5. B16 and HLA-A2-negative human melanoma SKMEL-3 were included as controls. C. HLA-A2 transgenic mice were inoculated subcutaneously on day 0 with 3 X 105 B16-A2 cells, and vaccinated intravenously on day7, and 14 with gp100209-pulsed HLA-A2 transgenic DCs and TriVax, respectively. A nonvaccinated group (No Vax) was also included
표
Establishment of HLA-A2-expressing mouse B16 (B16-A2) and C1498 (C1498-A2) cell lines. A. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry. B. HLA-A2 transgenic mice were immunized intravenously with gp100209 (ITDQVPFSV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. B. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining, and IFN-γ EliSpot assay against peptide-pulsed T2 (T2/gp100209), un-pulsed T2 cells, B16-A2, HLA-A2-positive human melanoma SKMEL-5. B16 and HLA-A2-negative human melanoma SKMEL-3 were included as controls. C. HLA-A2 transgenic mice were inoculated subcutaneously on day 0 with 3 X 105 B16-A2 cells, and vaccinated intravenously on day7, and 14 with gp100209-pulsed HLA-A2 transgenic DCs and TriVax, respectively. A nonvaccinated group (No Vax) was also included
 표
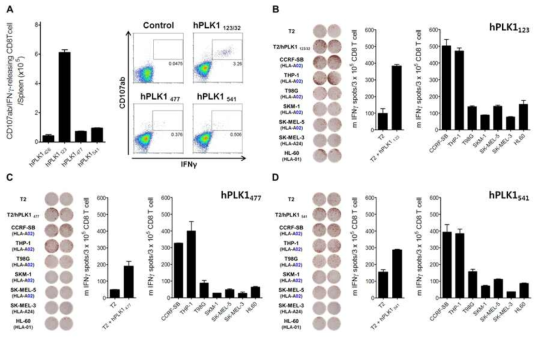
Validation of immunogenicity of putative PLK1-derived HLA-A2 epitopes using DCs prime/TriVax immunization strategy in HLA-A2 transgenic mice. HLA-A2 transgenic mice were immunized intravenously with either PLK112 (NDFVFVVLEL), PLK1477 (TLLKYFRNYM), or PLK1541 (LILCPLMAAV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. A. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigenspecific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed T2 cells as indicated, HLA-A2-positive CCRF-SB, THP-1, T98G, SKM-1, and SK-MEL-5 cells
표
Validation of immunogenicity of putative PLK1-derived HLA-A2 epitopes using DCs prime/TriVax immunization strategy in HLA-A2 transgenic mice. HLA-A2 transgenic mice were immunized intravenously with either PLK112 (NDFVFVVLEL), PLK1477 (TLLKYFRNYM), or PLK1541 (LILCPLMAAV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. A. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigenspecific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed T2 cells as indicated, HLA-A2-positive CCRF-SB, THP-1, T98G, SKM-1, and SK-MEL-5 cells
 표
Comparison of CD8 T cell responses induced with TriVax booster immunization after priming with peptide-loaded DCs or T cells. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs or T cells (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 μg Trp1455/9M, 50 μg poly-IC, and 100 μg anti-CD40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
표
Comparison of CD8 T cell responses induced with TriVax booster immunization after priming with peptide-loaded DCs or T cells. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs or T cells (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 μg Trp1455/9M, 50 μg poly-IC, and 100 μg anti-CD40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
 표
Expression of GFP on activated T cells in various conditions. Freshly isolated T cells from spleen using immunomagnetic beads were pre-activated with indicated conditions for 2 days. The ex vivo activated T cells were transduced with recombinant retroviruses encoding GFP, which were generated using pMys, pMSCV, and pMP71 vectors (pMys-GFP, pMSCV-GFP, and pMP71-GFP, respectively), followed by culturing in presence of 500U/ml IL-2. The expression of GFP on genetically modified T cells were chased for 10 days as indicated. The cells from each group were harvested and the expression of GFP analyzed by flow cytometry
표
Expression of GFP on activated T cells in various conditions. Freshly isolated T cells from spleen using immunomagnetic beads were pre-activated with indicated conditions for 2 days. The ex vivo activated T cells were transduced with recombinant retroviruses encoding GFP, which were generated using pMys, pMSCV, and pMP71 vectors (pMys-GFP, pMSCV-GFP, and pMP71-GFP, respectively), followed by culturing in presence of 500U/ml IL-2. The expression of GFP on genetically modified T cells were chased for 10 days as indicated. The cells from each group were harvested and the expression of GFP analyzed by flow cytometry
 표
Expression of costimulatory ligands OX40L, CD70, and OX40L/CD70 on activated T-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse OX40L, CD70, and OX40L/CD70. The OX40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pMSGV retroviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated T-cells were transduced with recombinant retroviruses encoding GFP, OX40L, CD70, and OX40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
표
Expression of costimulatory ligands OX40L, CD70, and OX40L/CD70 on activated T-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse OX40L, CD70, and OX40L/CD70. The OX40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pMSGV retroviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated T-cells were transduced with recombinant retroviruses encoding GFP, OX40L, CD70, and OX40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
 표
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with genetically modified T cells. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, CD80, 4-1BBL, and OX40L (GFP-T, CD70-T, CD80-T, 4-1BBL-T, and OX40L-T, respectively). B6 mice were immunized intravenously with either Trp1455-pulsed variously conditioned T cells (prime); 7 days later, the mice received a TriVax booster immunization. B. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ and CD107a/b staining after coculturing with Trp1455 peptide. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated for their capacity to recognize target cells using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
표
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with genetically modified T cells. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, CD80, 4-1BBL, and OX40L (GFP-T, CD70-T, CD80-T, 4-1BBL-T, and OX40L-T, respectively). B6 mice were immunized intravenously with either Trp1455-pulsed variously conditioned T cells (prime); 7 days later, the mice received a TriVax booster immunization. B. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ and CD107a/b staining after coculturing with Trp1455 peptide. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated for their capacity to recognize target cells using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
 표
Peptide-based booster immunization after priming with CD70-T-cells drives enhanced CD8 T-cell responses. B6 mice (2 per group) were immunized intravenously on day 0 with 2 × 106 Trp1455/9M-loaded CD70-T-cells; 7-days later, the mice received a booster immunization with various combination of 100 μg of Trp1455/9M peptide, 50 μg of poly-IC, and 50 μg anti-CD40, anti-4-1BB, or anti-OX40Abs. A. 7-days after last immunization, the frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
표
Peptide-based booster immunization after priming with CD70-T-cells drives enhanced CD8 T-cell responses. B6 mice (2 per group) were immunized intravenously on day 0 with 2 × 106 Trp1455/9M-loaded CD70-T-cells; 7-days later, the mice received a booster immunization with various combination of 100 μg of Trp1455/9M peptide, 50 μg of poly-IC, and 50 μg anti-CD40, anti-4-1BB, or anti-OX40Abs. A. 7-days after last immunization, the frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
 표
PD-L1 blockade augments the therapeutic efficacy of CD70-T_TriVax vaccination. A. Therapeutic efficacy of CD70-T_TriVax vaccination against advanced B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells, followed by vaccination with 2 × 106 GFP-T or CD70-T-cells on day 7, and TriVax on day 14. Non-vaccinated mice (No vax) and DC_TriVax were included for comparison. B. PD-L1 blockade enhanced the efficacy of CD70-T_TriVax vaccination regimen. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized as described above. Rat IgG (as controls) and anti-PD-L1 Abs were administered intraperitoneally on days +1 and +3 after each immunization. No vaccinated (No Vax) and Ova55-loaded CD70-T_TriVax vaccinated mice (Ova55) were included for comparison. C-E. In a parallel with B, mice were sacrificed on day 21, and the CD8 T-cell responses and immune cell populations were evaluated. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells per percentage of CD4+ Foxp3+T-cells in each group. D. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. E. Quantification of Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in tumor sites
표
PD-L1 blockade augments the therapeutic efficacy of CD70-T_TriVax vaccination. A. Therapeutic efficacy of CD70-T_TriVax vaccination against advanced B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells, followed by vaccination with 2 × 106 GFP-T or CD70-T-cells on day 7, and TriVax on day 14. Non-vaccinated mice (No vax) and DC_TriVax were included for comparison. B. PD-L1 blockade enhanced the efficacy of CD70-T_TriVax vaccination regimen. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized as described above. Rat IgG (as controls) and anti-PD-L1 Abs were administered intraperitoneally on days +1 and +3 after each immunization. No vaccinated (No Vax) and Ova55-loaded CD70-T_TriVax vaccinated mice (Ova55) were included for comparison. C-E. In a parallel with B, mice were sacrificed on day 21, and the CD8 T-cell responses and immune cell populations were evaluated. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells per percentage of CD4+ Foxp3+T-cells in each group. D. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining after coculturing with Trp1455 peptide. E. Quantification of Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in tumor sites
 표
Evaluation of heterogenous vaccination regimen with genetically modified T cell co-expressing OX40L and CD70. A. T cells were transduced individually or together with recombinant retroviruses encoding GFP, CD70, and OX40L as indicated (GFP-T, CD70-T, OX40L-T, and OX40L/CD70-T, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
표
Evaluation of heterogenous vaccination regimen with genetically modified T cell co-expressing OX40L and CD70. A. T cells were transduced individually or together with recombinant retroviruses encoding GFP, CD70, and OX40L as indicated (GFP-T, CD70-T, OX40L-T, and OX40L/CD70-T, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
 표
Expression of additional costimulatory ligands CD70, OX40L, and 4-1BBL on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD70, OX40L, and 4-1BBL. The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
표
Expression of additional costimulatory ligands CD70, OX40L, and 4-1BBL on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD70, OX40L, and 4-1BBL. The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
 표
Induction of antigen-specific CD8 T cell responses using heterogenous immunization after priming with peptide-loaded B cells, which are transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually (GFP-B, CD70-B, Ox40L-B, and 4-1BBL-B, respectively). B6 mice were immunized intravenously with Trp2180-pulsed variously conditioned B cells (prime); 7 days later, the mice received a booster immunization with TriVax. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp2180 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma
표
Induction of antigen-specific CD8 T cell responses using heterogenous immunization after priming with peptide-loaded B cells, which are transduced with recombinant lentiviruses encoding GFP, CD70, OX40L, 4-1BBL individually (GFP-B, CD70-B, Ox40L-B, and 4-1BBL-B, respectively). B6 mice were immunized intravenously with Trp2180-pulsed variously conditioned B cells (prime); 7 days later, the mice received a booster immunization with TriVax. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp2180 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. The presence of antigen-specific CD8 T-cells in the spleen was evaluated using IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma
 표
Expression of costimulatory ligands CD40L, and CD40L/CD70 on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD40L, and CD40L/CD70. The CD40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
표
Expression of costimulatory ligands CD40L, and CD40L/CD70 on activated B-cells. A. Schematic diagram of the constructs with costimulatory ligands mouse CD40L, and CD40L/CD70. The CD40L and CD70 were linked using specific primers to fuse a 2A coding sequence (ATNFSLLKQAGDVEENPGP).The cDNA encoding the interest genes are derived from mature DCs by extracting RNA using with BspEI and SalI restriction site hanging at the 5' and 3' terminal respectively. The amplified genes are then inserted into the pCDH-EF1 lentiviral vector. Green fluorescence protein (GFP) was used as control. B. Ex vivo activated B-cells were transduced with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70, respectively. Twenty-four hours post-transduction, cells from each group were harvested and the expression of costimulatory molecules analyzed by flow cytometry
 표
Evaluation of heterogenous vaccination regimen with genetically modified B cell co-expressing CD40L and CD70. A. T cells were transduced individually or together with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70 (GFP-B, CD40L-B, and CD40L/CD70-B, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 7 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
표
Evaluation of heterogenous vaccination regimen with genetically modified B cell co-expressing CD40L and CD70. A. T cells were transduced individually or together with recombinant lentiviruses encoding GFP, CD40L, and CD40L/CD70 (GFP-B, CD40L-B, and CD40L/CD70-B, respectively). To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 7 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp2180), un-pulsed EL4 cells (negative control), and B16 melanoma (B and C)
 표
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with DNA plasmid constructs encoding Survivin (A) or polo-like kinase (PLK1; B). Mice (3 per group) were vaccinated intramuscularly. with DNA plasmid followed immediately by electroporation of the injected area (95 V, 4 X 65 ms pulses with repoling) using TX830 Electro Square Porator device. 14 days later, the mice received a booster immunization with TriVax composed of 100 mg of peptide (as indicated), 50mg of poly-IC, and 100 mg of anti-CD40. 7 days later after last immunization, blood sample were evaluated by intracellular IFNγ staining, and total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. CD8 T cells were purified from pooled splenocytes of mice primed differently either peptide-loaded DC or DNA plasmids, and antigen-induced IFNγ secretion to PLK1122 (DSDFVFVVL) peptide was evaluated in EliSpot assays using peptide-pulsed APCs and B16 melanoma
표
Induction of antigen-specific CD8 T cell responses using heterogenous TriVax booster immunization after priming with DNA plasmid constructs encoding Survivin (A) or polo-like kinase (PLK1; B). Mice (3 per group) were vaccinated intramuscularly. with DNA plasmid followed immediately by electroporation of the injected area (95 V, 4 X 65 ms pulses with repoling) using TX830 Electro Square Porator device. 14 days later, the mice received a booster immunization with TriVax composed of 100 mg of peptide (as indicated), 50mg of poly-IC, and 100 mg of anti-CD40. 7 days later after last immunization, blood sample were evaluated by intracellular IFNγ staining, and total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated. C. CD8 T cells were purified from pooled splenocytes of mice primed differently either peptide-loaded DC or DNA plasmids, and antigen-induced IFNγ secretion to PLK1122 (DSDFVFVVL) peptide was evaluated in EliSpot assays using peptide-pulsed APCs and B16 melanoma
 표
Mul-ti-epitope-coding DNA priming followed by TriVax boost with multi-peptides induces concurrent CD8 T cell responses. A. Multi-epitope plasmid constructs coding three CD8 T cell epitopes for melanosomal antigens and a CD4 T cell epitope OT2 linked with furin-sensitive (RVKR) or furin-insensitive spacer (VRVV). B and C. Induction of antigen-specific CD8 T cell responses using DNA plasmid encoding multi-epitopes drived from melanosomal antigens. Anesthetized mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830 device. 14 days later, the mice were received booster immunization. B. 8 days after the boost, the presence of antigen-specific CD8 T cell responses in spleen were evaluated by intracellular IFNγ staining after coculturing with individual peptides (Ova257, Trp1455, Trp2180, Hugp10025, and Mogp10025). C. Freshly isolated CD8 T ells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, and EL4/mgp10025, respectively), and un-pulsed EL4
표
Mul-ti-epitope-coding DNA priming followed by TriVax boost with multi-peptides induces concurrent CD8 T cell responses. A. Multi-epitope plasmid constructs coding three CD8 T cell epitopes for melanosomal antigens and a CD4 T cell epitope OT2 linked with furin-sensitive (RVKR) or furin-insensitive spacer (VRVV). B and C. Induction of antigen-specific CD8 T cell responses using DNA plasmid encoding multi-epitopes drived from melanosomal antigens. Anesthetized mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830 device. 14 days later, the mice were received booster immunization. B. 8 days after the boost, the presence of antigen-specific CD8 T cell responses in spleen were evaluated by intracellular IFNγ staining after coculturing with individual peptides (Ova257, Trp1455, Trp2180, Hugp10025, and Mogp10025). C. Freshly isolated CD8 T ells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, and EL4/mgp10025, respectively), and un-pulsed EL4
 표
Induction of antigen-specific CD8 T cell responses on HLA-A2 transgeneic mice using synthetic DNA plasmid encoding putative HLA-A2-restricted multi-epitopes drived from human PLK1. Mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA, injected three times at interval of 7 days, followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830. 8 days after the last immunization, the presence of antigen-specific CD8 T cell responses in spleen were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 as indicated, and un-pulsed EL4 cells (negative control)
표
Induction of antigen-specific CD8 T cell responses on HLA-A2 transgeneic mice using synthetic DNA plasmid encoding putative HLA-A2-restricted multi-epitopes drived from human PLK1. Mice were vaccinated intramuscularly with a total of 100 μg of plasmid DNA, injected three times at interval of 7 days, followed immediately by electroporation (95 V, 4 X65 ms pulses with repoling) using TX830. 8 days after the last immunization, the presence of antigen-specific CD8 T cell responses in spleen were evaluated for antigen-induced IFNγ secretions with peptide-pulsed EL4 as indicated, and un-pulsed EL4 cells (negative control)
 표
Comparison of CD8 T cell responses induced with TriVax booster immunization, which are composed with anti-CD40 or anti-OX40 in DC-prime/TriVax-boost vaccination regime. B6 mice (2 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs; 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 50mg of poly-IC, and 100 mg of either anti-CD40 or anti-Ox40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells from pooled splenocytes was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
표
Comparison of CD8 T cell responses induced with TriVax booster immunization, which are composed with anti-CD40 or anti-OX40 in DC-prime/TriVax-boost vaccination regime. B6 mice (2 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs; 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 50mg of poly-IC, and 100 mg of either anti-CD40 or anti-Ox40. A. On day 14 (post-boost), blood sample were evaluated by intracellular IFNγ staining after coculturing with Trp1455 peptide. B. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. C. CD8 T cells from pooled splenocytes was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Trp1455), B16 melanoma
 표
Effect of TLR-Ls on heterogenous peptide-loaded DC prime/TriVax boost regime. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 100 mg of anti-CD40, and one of the following TLR-L: Poly-IC (TLR3-L), CpG (TLR9-L), LPS (TLR4-L), Pam2CSk4 (TLR2-L), and GDQ (TLR7-L). The frequency of Trp1455-specific CD8 T cells in peripheral blood was evaluated by intracellular IFNγ staining in individual mice for 2 weeks (on day 14 and 21)
표
Effect of TLR-Ls on heterogenous peptide-loaded DC prime/TriVax boost regime. B6 mice (3 per group) were immunized intravenously with either Trp1455/9M peptide-pulsed DCs (prime); 7 days later, the mice received a booster immunization with TriVax composed of 100 mg of Trp1455/9M, 100 mg of anti-CD40, and one of the following TLR-L: Poly-IC (TLR3-L), CpG (TLR9-L), LPS (TLR4-L), Pam2CSk4 (TLR2-L), and GDQ (TLR7-L). The frequency of Trp1455-specific CD8 T cells in peripheral blood was evaluated by intracellular IFNγ staining in individual mice for 2 weeks (on day 14 and 21)
 표
Multi-epitope-loaded CD70-T-cells priming followed by TriVax booster immunization induces concurrent effective antitumor CD8 T cell responses. B6 mice were immunized intravenously with CD70-T-cells that were loaded with mixture of Trp1455/9M, Trp2180, and hgp10025 peptides; 7-days later, the mice received 3pepMIXTriVax. A. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455, Trp2180, mgp10025-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, EL4/mgp10025), B16 melanoma. C. Therapeutic effectiveness of multi-epitope-loaded CD70-T_TriVax immunization against 3-day-established B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized intravenously on day 3, and 10 in combination with CD70-T or TriVax using either individual peptide or mixture of Trp1455/9M, Trp2180, and hgp10025 (3pepMIX) peptides as indicated
표
Multi-epitope-loaded CD70-T-cells priming followed by TriVax booster immunization induces concurrent effective antitumor CD8 T cell responses. B6 mice were immunized intravenously with CD70-T-cells that were loaded with mixture of Trp1455/9M, Trp2180, and hgp10025 peptides; 7-days later, the mice received 3pepMIXTriVax. A. The frequency of antigen-specific CD8 T-cells in spleen was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. B. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes and antigen-induced IFNγ secretion was evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: Trp1455, Trp2180, mgp10025-pulsed EL4 (EL4/Trp1455, EL4/Trp2180, EL4/mgp10025), B16 melanoma. C. Therapeutic effectiveness of multi-epitope-loaded CD70-T_TriVax immunization against 3-day-established B16 melanoma. B6 mice were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and were immunized intravenously on day 3, and 10 in combination with CD70-T or TriVax using either individual peptide or mixture of Trp1455/9M, Trp2180, and hgp10025 (3pepMIX) peptides as indicated
 표
Induction of PLK1–specific CD8 T cell responses using DCs prime/TriVax immunization regimen in C57BL/6j mice. Mice were vaccinated i.v. on day 0 with DCs loaded with each peptide, mPLK1122 (DSDFVFVVL), mPLK1262 (RIKKNEYSI), mPLK1332 (LDPSSRKPL), mPLK1345 (KGVENPLPD) for priming. 7 days later, the mice were received booster immunizatin with TriVax composed 150 μg of peptide, 50 μg of poly-IC, and 100 μg of anti-CD40. A. Eight days after the boost, splenocytes from each individual mouse were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells (B), B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells (C-D) as indicated. Un-pulsed EL4 cells were used as controls
표
Induction of PLK1–specific CD8 T cell responses using DCs prime/TriVax immunization regimen in C57BL/6j mice. Mice were vaccinated i.v. on day 0 with DCs loaded with each peptide, mPLK1122 (DSDFVFVVL), mPLK1262 (RIKKNEYSI), mPLK1332 (LDPSSRKPL), mPLK1345 (KGVENPLPD) for priming. 7 days later, the mice were received booster immunizatin with TriVax composed 150 μg of peptide, 50 μg of poly-IC, and 100 μg of anti-CD40. A. Eight days after the boost, splenocytes from each individual mouse were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells (B), B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells (C-D) as indicated. Un-pulsed EL4 cells were used as controls
 표
DC-prime/TriVax vaccination with mPLK1122 epitopes results in strong antitumor effects against established C1498 leukemia. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122 or mPLK1345/9M-vaccinated group
표
DC-prime/TriVax vaccination with mPLK1122 epitopes results in strong antitumor effects against established C1498 leukemia. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122 or mPLK1345/9M-vaccinated group
 표
Memory antitumor effects of DC-prime/TriVax vaccination with mPLK1122 epitopes. A. At the termination of the experiment presented in Fig. 16, tumor-free (rejected) B6 mice (4 per group) received subcutaneous tumor rechallenge with 2 x 106 live luciferase-expressing C1498 (C1498/Luci) cells (in the opposite flank). Naïve, unvaccinated mice inoculated with the same number of C1498/Luci cells were included as controls
표
Memory antitumor effects of DC-prime/TriVax vaccination with mPLK1122 epitopes. A. At the termination of the experiment presented in Fig. 16, tumor-free (rejected) B6 mice (4 per group) received subcutaneous tumor rechallenge with 2 x 106 live luciferase-expressing C1498 (C1498/Luci) cells (in the opposite flank). Naïve, unvaccinated mice inoculated with the same number of C1498/Luci cells were included as controls
 표
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established Hepa1-6 hepatocacinoma. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing Hepa1-6 cells, and vaccinated intravenously as in Fig. 16. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122-vaccinated group
표
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established Hepa1-6 hepatocacinoma. B6 mice were inoculated subcutaneously on day 0 with 2 x 106 live luciferase-expresssing Hepa1-6 cells, and vaccinated intravenously as in Fig. 16. A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Tumor growth in mice treated with control (No Vax), OVA55, mPLK1122-vaccinated group
 표
Effects of CD70-T vaccination in antitumor efficacy of adoptive T-cell therapy. A-C. B6 mice were adoptively transferred 5 × 106 naive Pmel-1 T-cells on day 0, followed by immunization on day 1 with 3 × 106 hgp10025-pulsed GFP-T and CD70-T-cells. Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. A. 7-days after the immunization, in vivo expansion of Pmel-1 T-cells (CD90.1+ CD8 T-cells) in spleen was assessed. B. The frequency of mgp10025-specific CD8 T-cells was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. C. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes were evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: mgp10025-pulsed EL4 (EL4/mgp10025), B16 melanoma. D. Antitumor effects of CD70-T immunization after pmel-1 ACT. B6 mice (5 per group) were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and received 5 × 106 Pmel-1 cells on day 3 followed by vaccination with hgp10025-pulsed GFP-T and CD70-T-cells thrice (on day 4, 7, and 10: D, vertical arrows). For CD70-T_TriVax regimen, TriVax was administered intravenously 5-days after CD70-T vaccination. Non-vaccinated mice (No Vax), Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. E. In a parallel with D , respectively, mice (4 per group) were sacrificed on day 21, and the frequency of Pmel-1 T-cells in spleen and tumor site was evaluated
표
Effects of CD70-T vaccination in antitumor efficacy of adoptive T-cell therapy. A-C. B6 mice were adoptively transferred 5 × 106 naive Pmel-1 T-cells on day 0, followed by immunization on day 1 with 3 × 106 hgp10025-pulsed GFP-T and CD70-T-cells. Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. A. 7-days after the immunization, in vivo expansion of Pmel-1 T-cells (CD90.1+ CD8 T-cells) in spleen was assessed. B. The frequency of mgp10025-specific CD8 T-cells was evaluated by cell surface mobilization of CD107a/b and intracellular IFNγ staining. C. Antigen-induced IFNγ-secretions with freshly isolated CD8 T cells from pooled splenocytes were evaluated for their capacity to recognize tumor cells using EliSpot assay. APCs used: mgp10025-pulsed EL4 (EL4/mgp10025), B16 melanoma. D. Antitumor effects of CD70-T immunization after pmel-1 ACT. B6 mice (5 per group) were inoculated subcutaneously on day 0 with 1 × 105 B16 cells and received 5 × 106 Pmel-1 cells on day 3 followed by vaccination with hgp10025-pulsed GFP-T and CD70-T-cells thrice (on day 4, 7, and 10: D, vertical arrows). For CD70-T_TriVax regimen, TriVax was administered intravenously 5-days after CD70-T vaccination. Non-vaccinated mice (No Vax), Pmel-1 ACT alone (ACT only) and DC vaccinated mice (DC) were included for comparison. E. In a parallel with D , respectively, mice (4 per group) were sacrificed on day 21, and the frequency of Pmel-1 T-cells in spleen and tumor site was evaluated
 표
Combination of zoledonate on peptide-loaded DC-prime/TriVax booster immunization elicits enhanced CD8 T cell responses. B6 mice were immunized intravenously with Sur20 (ATFKNWPFL)-pulsed DC or TriVax; 7 days later, the mice received a combinatorial booster immunization. Zoledonate was administered on day 1 and 3 after vaccination. A and B. 8 days after the boost, the presence of Trp1455-specific CD8 T cells in spleen was evaluated by intracellular IFNγ staining after coculturing with Sur20 peptide. C. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. D and E. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Sur20), C1498 acute myeloid leukemia, B16 melanoma, MC38 colon adenocarcinoma, GL26 glioblastoma, Tramp-C2, prostate adenocarcinoma, and Hepa1-6 hepatoma
표
Combination of zoledonate on peptide-loaded DC-prime/TriVax booster immunization elicits enhanced CD8 T cell responses. B6 mice were immunized intravenously with Sur20 (ATFKNWPFL)-pulsed DC or TriVax; 7 days later, the mice received a combinatorial booster immunization. Zoledonate was administered on day 1 and 3 after vaccination. A and B. 8 days after the boost, the presence of Trp1455-specific CD8 T cells in spleen was evaluated by intracellular IFNγ staining after coculturing with Sur20 peptide. C. Total numbers of intracellular IFNγ and cell surface CD107a/b double-positive CD8 T cells was calculated from the experiment in A. D and E. CD8 T cells were purified from pooled splenocytes, and antigen-induced IFNγ secretion was evaluated using EliSpot assay. APCs used: Trp1455-pulsed EL4 (EL4/Sur20), C1498 acute myeloid leukemia, B16 melanoma, MC38 colon adenocarcinoma, GL26 glioblastoma, Tramp-C2, prostate adenocarcinoma, and Hepa1-6 hepatoma
 표
Combined effects of zoledonate (ZA) on therapeutic immunity in DC prime-TriVax boost vaccination strategy against established C1498 leukemia. A and B. B6 mice (4 per group) were inoculated subcutaneously on day 0 with 3 X 105 C1498 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, Pamidronate (PA), and anti-PD-L1 was administered on day 1 and 3 after vaccination. A. Effects of ZA in combinatorial vaccination on the therapeutic efficacy of antigen-loaded DCs and TriVax immunization. B and C. For leukemic tumor model, B6 mice were infused intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated on day 7 and 14. Time course of bioluminescence in individual mice from both treatment groups
표
Combined effects of zoledonate (ZA) on therapeutic immunity in DC prime-TriVax boost vaccination strategy against established C1498 leukemia. A and B. B6 mice (4 per group) were inoculated subcutaneously on day 0 with 3 X 105 C1498 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, Pamidronate (PA), and anti-PD-L1 was administered on day 1 and 3 after vaccination. A. Effects of ZA in combinatorial vaccination on the therapeutic efficacy of antigen-loaded DCs and TriVax immunization. B and C. For leukemic tumor model, B6 mice were infused intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated on day 7 and 14. Time course of bioluminescence in individual mice from both treatment groups
 표
Zoledronate and PD1 blockade revealed synergic therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established B16 melanoma. A and B. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated using either Sur20 (ATFKNWPFL: A) or Trp1455/9M (TAPDNLGYM: B). ZA and anti-PD-L1 was administered on day 1 and 3 after vaccination. C. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
표
Zoledronate and PD1 blockade revealed synergic therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established B16 melanoma. A and B. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated using either Sur20 (ATFKNWPFL: A) or Trp1455/9M (TAPDNLGYM: B). ZA and anti-PD-L1 was administered on day 1 and 3 after vaccination. C. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
 표
Rapamycin enhance the therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14. Rapamycin wwas administered intraperitoneally (1 mg/kg) for three days after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry
표
Rapamycin enhance the therapeutic efficacy of DC-TriVax heterologous vaccination regimen against established C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14. Rapamycin wwas administered intraperitoneally (1 mg/kg) for three days after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry
 표
Expression and biological function of TCR-engineered T cells transduced with gp10025-specific (pmel) mTCR, which was cloned together with IRES or T2A linker. A. Flow cytometric analysis of gp10025-specific mTCR-transduced mouse T cells. B-C. The antigen-specificity of pmel TCR-engineered T cells was evaluated by IFNγ EliSpot or ELISA assay with peptide-pulsed EL4 cells, B16 melanoma as indicated. The peptides gp10025 (KVPRNQDWL), mgp10025 (EGSRNQDWL), or Trp1455 (TAPDNLGYA) were used for pulsing on EL4 cells. Un-pulsed EL4 cells were used as controls
표
Expression and biological function of TCR-engineered T cells transduced with gp10025-specific (pmel) mTCR, which was cloned together with IRES or T2A linker. A. Flow cytometric analysis of gp10025-specific mTCR-transduced mouse T cells. B-C. The antigen-specificity of pmel TCR-engineered T cells was evaluated by IFNγ EliSpot or ELISA assay with peptide-pulsed EL4 cells, B16 melanoma as indicated. The peptides gp10025 (KVPRNQDWL), mgp10025 (EGSRNQDWL), or Trp1455 (TAPDNLGYA) were used for pulsing on EL4 cells. Un-pulsed EL4 cells were used as controls
 표
Effects of peptide-based vaccines on the expansion of adoptively transferred pmel T cells. B6 mice were adoptively transferred with 2 ⨯ 106 naive Pmel T cells followed by immunization one day later with various combinations of 100 mg of hgp10025 peptide, 50 mg of poly-IC, 100 mg of anti-CD40, anti-4.1BB, and anti-OX40 Abs as indicated. Eight days later, splenocytes from each mouse were examined for the expansion of pmel T cells (A), and antigen-specific recognition by intracellular IFNγ staining after coculturing with hgp10025 peptide (B) and EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma as indicated (C). D. Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
표
Effects of peptide-based vaccines on the expansion of adoptively transferred pmel T cells. B6 mice were adoptively transferred with 2 ⨯ 106 naive Pmel T cells followed by immunization one day later with various combinations of 100 mg of hgp10025 peptide, 50 mg of poly-IC, 100 mg of anti-CD40, anti-4.1BB, and anti-OX40 Abs as indicated. Eight days later, splenocytes from each mouse were examined for the expansion of pmel T cells (A), and antigen-specific recognition by intracellular IFNγ staining after coculturing with hgp10025 peptide (B) and EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma as indicated (C). D. Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
 표
Heterologous vaccination with mPLK1122-DC-prime/TriVax prolongs survival of mice with C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. For PD-1 blockade, anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Kaplan–Mayer survival curves for all groups of mice. D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells as indicated. Un-pulsed EL4 cells were used as controls
표
Heterologous vaccination with mPLK1122-DC-prime/TriVax prolongs survival of mice with C1498 leukemia. B6 mice were inoculated intravenously on day 0 with 2 x 106 live luciferase-expresssing C1498 cells, and vaccinated intravenously on day 7 and 14 with peptide-pulsed DC and TriVax, respectively. For PD-1 blockade, anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after each immunization (prime and boost). A non-vaccinated group (No Vax) was included as controls. A. Time course of bioluminescence (BLI) in representative individual mice from all treatment groups. B. Tumour growth was monitored by in vivo bioluminescence imaging. C. Kaplan–Mayer survival curves for all groups of mice. D. The presence of antigen-specific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed EL4 cells, B16 melanoma, Hepa1-6 hepatoma, and C1498 leukemia cells as indicated. Un-pulsed EL4 cells were used as controls
 표
Effects of PD-L1 blockade on the therapeutic efficacy of PLK1122 DC_TriVax vaccination. In a parallel with Figure 1A, mice (3 per group) were sacrificed on day23, and the tissues and cells from disaggregated tissues were evaluated for the antitumor CD8 T-cell responses and immune cell populations. A. Frequency of PLK1122-specific CD8 T-cells in spleen was evaluated by intracellular IFNγ staining. Points, value for each individual mouse; horizontal line, average of the group. B. Freshly isolated CD8 T-cells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions by EliSpot against indicated target cells. Results represent the average number of spots from triplicate wells with SD (bars) of the means. C-G. Cells from disaggregated tissues of liver, bone-marrow (BM), spleen, and lung were analyzed by flow cytometry for the composition of tumor cells and various subsets of immune cells. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells/ percentage of CD4+ Foxp3+T-cells. D. Infiltration of (CD90.1-positive) C1498 leukemic cells. E. Representative flow cytometric plots showing Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in liver tissue. Results represent the average percentage of the gated cells from individual mice with SD (bars) of the means. P values were calculated using unpaired Student's t tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). These experiments were repeated twice with similar results
표
Effects of PD-L1 blockade on the therapeutic efficacy of PLK1122 DC_TriVax vaccination. In a parallel with Figure 1A, mice (3 per group) were sacrificed on day23, and the tissues and cells from disaggregated tissues were evaluated for the antitumor CD8 T-cell responses and immune cell populations. A. Frequency of PLK1122-specific CD8 T-cells in spleen was evaluated by intracellular IFNγ staining. Points, value for each individual mouse; horizontal line, average of the group. B. Freshly isolated CD8 T-cells from pooled splenocytes were evaluated for antigen-induced IFNγ secretions by EliSpot against indicated target cells. Results represent the average number of spots from triplicate wells with SD (bars) of the means. C-G. Cells from disaggregated tissues of liver, bone-marrow (BM), spleen, and lung were analyzed by flow cytometry for the composition of tumor cells and various subsets of immune cells. C. CD8 T-cell/Treg ratio as measured by percentage of CD8+ T-cells/ percentage of CD4+ Foxp3+T-cells. D. Infiltration of (CD90.1-positive) C1498 leukemic cells. E. Representative flow cytometric plots showing Ly6GlowLy6Chigh monocytic myeloid-derived suppressor cells (M-MDSC) and Ly6GhighLy6Clow granulocytic polymorphonuclear MDSC (PMN-MDSC) gated on CD11b+CD115high myeloid cells in liver tissue. Results represent the average percentage of the gated cells from individual mice with SD (bars) of the means. P values were calculated using unpaired Student's t tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). These experiments were repeated twice with similar results
 표
DCs priming followed by TriVax boost with multi-peptides with sustained PD-L1 blockade elicits augmented therapeutic effectiveness overcoming clonal heterogeneity of C1498 leukemia. B6 mice (6 to 10 per group) were intravenously 2×106 C1498-luc cells, and received DC_TriVax immunization using either individual peptide or mixture of PLK1122 and Sur20 (as indicated) with prolonged period of PD-L1 blockade, followed by weekly bioluminescence imaging. Non-vaccinated mice (No Vax) and Ova55DC_TriVax-vaccinated mice (Ova55) were included as controls. Anti-PD-L1 was administered three-times (x3) on days +1, +3 and +5 for long-term treatment after each immunization. A. Tumor growth was monitored by time course of in vivo bioluminescence imaging in individual mice (left panel), and average radiance per mouse is shown (right panel). Images were adjusted to the same pseudo color scale to show relative bioluminescence changes over time. Points, average values of photons in mouse; bars, SD. B. Kaplan-Mayer survival curves for all groups of mice in A. P values were determined by log-rank tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). C. Frequency of PLK1122-specific CD8T-cellswasevaluatedbyintracellularIFNg staining on day45 using blood samples from mice in A. Points, value for each individual mouse; horizontal line, average of the group. P values were calculated using unpaired Student’s t test (***, P <0.01). These experiments were repeated twice with similar results
표
DCs priming followed by TriVax boost with multi-peptides with sustained PD-L1 blockade elicits augmented therapeutic effectiveness overcoming clonal heterogeneity of C1498 leukemia. B6 mice (6 to 10 per group) were intravenously 2×106 C1498-luc cells, and received DC_TriVax immunization using either individual peptide or mixture of PLK1122 and Sur20 (as indicated) with prolonged period of PD-L1 blockade, followed by weekly bioluminescence imaging. Non-vaccinated mice (No Vax) and Ova55DC_TriVax-vaccinated mice (Ova55) were included as controls. Anti-PD-L1 was administered three-times (x3) on days +1, +3 and +5 for long-term treatment after each immunization. A. Tumor growth was monitored by time course of in vivo bioluminescence imaging in individual mice (left panel), and average radiance per mouse is shown (right panel). Images were adjusted to the same pseudo color scale to show relative bioluminescence changes over time. Points, average values of photons in mouse; bars, SD. B. Kaplan-Mayer survival curves for all groups of mice in A. P values were determined by log-rank tests (ns, not significant; *, P <0.05; **, P <0.01; ***, P <0.001). C. Frequency of PLK1122-specific CD8T-cellswasevaluatedbyintracellularIFNg staining on day45 using blood samples from mice in A. Points, value for each individual mouse; horizontal line, average of the group. P values were calculated using unpaired Student’s t test (***, P <0.01). These experiments were repeated twice with similar results
 표
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established B16 melanoma. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 and anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after vaccination. B. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
표
Therapeutic antitumor effects of mPLK1122-DC-prime/TriVax vaccination regimen gainst established B16 melanoma. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 and anti-PD-L1 Abs were administered intraperitoneally (200 μg/dose) on days 0 and 2 after vaccination. B. B6 mice received 3 × 105 B16 cells intravenously and vaccinated intravenously with on day7, and 14. A nonvaccinated group (No Vax) was also included. On day 24, the presence of B16 pulmonary nodules was evaluated. Results are presented as “No. lung tumors ” and “Lung weights” for individual mice. Representative photographs of lungs of two mice from each group are shown
 표
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing IL21. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, and IL21 as indicated (GFP-T, CD70-T, and IL21-T, respectively). B. The secretion of IL21 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (C and D)
표
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing IL21. A. T cells were transduced with recombinant retroviruses encoding GFP, CD70, and IL21 as indicated (GFP-T, CD70-T, and IL21-T, respectively). B. The secretion of IL21 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma (C and D)
 표
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing CD70 and CXCR3. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70 and CXCR3 as indicated (CD70-T, CXCR3-T and CD70/CXCR3-T, respectively). B and C. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
표
Evaluation of heterogenous vaccination regimen with genetically modified T cells expressing CD70 and CXCR3. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70 and CXCR3 as indicated (CD70-T, CXCR3-T and CD70/CXCR3-T, respectively). B and C. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells (negative control), and B16 melanoma
 표
IL12-transduced T cells enhance the therapeutic efficacy of heterogenous vaccination regimen against established B16 melanoma. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70, IL12, and CXCR3 as indicated (CD70-T, IL12-T, CD70/IL12-T, and CD70/IL12/CXCR3-T, respectively). B. The secretion of IL12 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells, and B16 melanoma (C and D). For the therapeutic efficacy, B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 according to heterogenous vaccination regimen
표
IL12-transduced T cells enhance the therapeutic efficacy of heterogenous vaccination regimen against established B16 melanoma. A. T cells were transduced individually or together with recombinant retroviruses encoding CD70, IL12, and CXCR3 as indicated (CD70-T, IL12-T, CD70/IL12-T, and CD70/IL12/CXCR3-T, respectively). B. The secretion of IL12 from gene-transferred T cells was measured using Elisa assay. To evaluate the antigen-specific CD8 T-cell responses, B6 mice were immunized and examined as in Fig. 4 using intracellular IFNγ and CD107a/b staining and IFN-γ EliSpot assay against peptide-pulsed EL4 (EL4/Trp1455), un-pulsed EL4 cells, and B16 melanoma (C and D). For the therapeutic efficacy, B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 according to heterogenous vaccination regimen
 표
Zoledronate, PD-1 blockade and IL2Cx enhance the therapeutic efficacy of DCs prime-TriVax boost heterogenous vaccination regimen. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. Non-vaccinated mice (No Vax) and Ova55-loaded DCs prime-Ova55TriVax booster-vaccinated mice were included as controls. B. On day 24, the presence of peptide-specific CD8 T cells in tumor-infiltrating lymphocytes (TIL) and splenocytes (SPL) were evaluated by intracellular IFNγ and CD107a/b staining. C. B6 mice were immunized intravenously with Trp1455-pulsed DC (prime); 7 days later, the mice received a TriVax booster immunization and ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. On day 18 (post-boost), Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
표
Zoledronate, PD-1 blockade and IL2Cx enhance the therapeutic efficacy of DCs prime-TriVax boost heterogenous vaccination regimen. A. B6 mice were inoculated subcutaneously on day 0 with 3 X 105 B16 cells and vaccinated intravenously on day7, and 14 (vertical arrow) as indicated. ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. Non-vaccinated mice (No Vax) and Ova55-loaded DCs prime-Ova55TriVax booster-vaccinated mice were included as controls. B. On day 24, the presence of peptide-specific CD8 T cells in tumor-infiltrating lymphocytes (TIL) and splenocytes (SPL) were evaluated by intracellular IFNγ and CD107a/b staining. C. B6 mice were immunized intravenously with Trp1455-pulsed DC (prime); 7 days later, the mice received a TriVax booster immunization and ZA, IL2Cx or anti-PD-L1 was administered on day 1 and 3 after vaccination. On day 18 (post-boost), Cells from each group of mice of spleen (SPL), lymph-node (LN), and bone-marrow (BM) were also evaluated for their antigenic specificity by intracellular IFNγ staining
 표
Establishment of HLA-A2-expressing mouse B16 (B16-A2) and C1498 (C1498-A2) cell lines. A. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry. B. HLA-A2 transgenic mice were immunized intravenously with gp100209 (ITDQVPFSV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. B. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining, and IFN-γ EliSpot assay against peptide-pulsed T2 (T2/gp100209), un-pulsed T2 cells, B16-A2, HLA-A2-positive human melanoma SKMEL-5. B16 and HLA-A2-negative human melanoma SKMEL-3 were included as controls. C. HLA-A2 transgenic mice were inoculated subcutaneously on day 0 with 3 X 105 B16-A2 cells, and vaccinated intravenously on day7, and 14 with gp100209-pulsed HLA-A2 transgenic DCs and TriVax, respectively. A nonvaccinated group (No Vax) was also included
표
Establishment of HLA-A2-expressing mouse B16 (B16-A2) and C1498 (C1498-A2) cell lines. A. Expression levels of MHC-I (H-2Kb and H-2Db), MHC-II, and PD-L1 on B16 and IFNγ-treated B16 cells measured by flow cytometry. B. HLA-A2 transgenic mice were immunized intravenously with gp100209 (ITDQVPFSV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. B. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining, and IFN-γ EliSpot assay against peptide-pulsed T2 (T2/gp100209), un-pulsed T2 cells, B16-A2, HLA-A2-positive human melanoma SKMEL-5. B16 and HLA-A2-negative human melanoma SKMEL-3 were included as controls. C. HLA-A2 transgenic mice were inoculated subcutaneously on day 0 with 3 X 105 B16-A2 cells, and vaccinated intravenously on day7, and 14 with gp100209-pulsed HLA-A2 transgenic DCs and TriVax, respectively. A nonvaccinated group (No Vax) was also included
 표
Validation of immunogenicity of putative PLK1-derived HLA-A2 epitopes using DCs prime/TriVax immunization strategy in HLA-A2 transgenic mice. HLA-A2 transgenic mice were immunized intravenously with either PLK112 (NDFVFVVLEL), PLK1477 (TLLKYFRNYM), or PLK1541 (LILCPLMAAV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. A. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigenspecific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed T2 cells as indicated, HLA-A2-positive CCRF-SB, THP-1, T98G, SKM-1, and SK-MEL-5 cells
표
Validation of immunogenicity of putative PLK1-derived HLA-A2 epitopes using DCs prime/TriVax immunization strategy in HLA-A2 transgenic mice. HLA-A2 transgenic mice were immunized intravenously with either PLK112 (NDFVFVVLEL), PLK1477 (TLLKYFRNYM), or PLK1541 (LILCPLMAAV)-pulsed HLA-A2 transgenic DCs (prime); 7 days later, the mice received a TriVax. booster immunization. A. HLA-A2 transgenic splenocytes were stimulated for cell surface mobilization of CD107a/b and intracellular IFNγ staining. B-D. The presence of antigenspecific CD8 T cell reponses in spleen were evaluated by IFNγ EliSpot assay with peptide-pulsed T2 cells as indicated, HLA-A2-positive CCRF-SB, THP-1, T98G, SKM-1, and SK-MEL-5 cells
| 과제명(ProjectTitle) : | - |
|---|---|
| 연구책임자(Manager) : | - |
| 과제기간(DetailSeriesProject) : | - |
| 총연구비 (DetailSeriesProject) : | - |
| 키워드(keyword) : | - |
| 과제수행기간(LeadAgency) : | - |
| 연구목표(Goal) : | - |
| 연구내용(Abstract) : | - |
| 기대효과(Effect) : | - |
Copyright KISTI. All Rights Reserved.

※ AI-Helper는 부적절한 답변을 할 수 있습니다.