최소 단어 이상 선택하여야 합니다.
최대 10 단어까지만 선택 가능합니다.
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
NTIS 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
DataON 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Edison 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Kafe 바로가기
| 주관연구기관 | 서울대학교 Seoul National University |
|---|---|
| 보고서유형 | 최종보고서 |
| 발행국가 | 대한민국 |
| 언어 | 한국어 |
| 발행년월 | 2014-04 |
| 과제시작연도 | 2013 |
| 주관부처 | 미래창조과학부 Ministry of Science, ICT and Future Planning |
| 등록번호 | TRKO201500002467 |
| 과제고유번호 | 1345199242 |
| 사업명 | 중견연구자지원 |
| DB 구축일자 | 2015-05-16 |
| 키워드 | 생체시계유전자.활성산소종.지방간.지방간염.Rev-erb.ROR.CCG (clock controlled gene).LXR.AMPK.ROS.Fatty liver.Steatohepatitis. |
| DOI | https://doi.org/10.23000/TRKO201500002467 |
연구의 목적 및 내용
생체시계 핵심 조절자 Rev-erbα/RORα의 상호작용이 hepatic steatosis에서 지질 합성 및 산회 경로와 활성 산소종의 생성과 제거에 미치는 영향과 그 분자생물학적 기전을 밝히고, 생체시계 유전자와 지질 대사의 통합적인 조절 기전을 밝히고자 하였다. 또한 Rev-erbα/RORα의 저분자 리간드와 genetic mutant mouse model를 개발하여 Rev-erbα/RORα의 병태생리학적 역할과 지질대사와 염증의 개선의 효과를 분석하여 간 대사성 질환 개선의 약학적 기반을 확립하는데
연구의 목적 및 내용
생체시계 핵심 조절자 Rev-erbα/RORα의 상호작용이 hepatic steatosis에서 지질 합성 및 산회 경로와 활성 산소종의 생성과 제거에 미치는 영향과 그 분자생물학적 기전을 밝히고, 생체시계 유전자와 지질 대사의 통합적인 조절 기전을 밝히고자 하였다. 또한 Rev-erbα/RORα의 저분자 리간드와 genetic mutant mouse model를 개발하여 Rev-erbα/RORα의 병태생리학적 역할과 지질대사와 염증의 개선의 효과를 분석하여 간 대사성 질환 개선의 약학적 기반을 확립하는데 기여하고자 하였다.
연구결과
제 1 단계: 생체시계유전자 Rev-erbα/RORα와 지질대사의 통합적 조절 기전 규명
1) 1차년도 Rev-erbα/RORα과 지질합성의 주요 경로인 LXR/SREBP-1/FAS 신호계와의 상호 작용 규명: Rev-erbα/RORα에 의해 LXR/SREBP-1/FAS 경로가 증대 또는 억제되고, LXR의 전사활성이 조절된다. 간세포에서 LXR 활성화로 인해 유도되는 lipid droplets 생성에 Rev-erbα/RORα이 기여 또는 저해하는 역할을 하며, LXR/SREBP-1/ FAS 경로 활성화는 Bmal1, Per 등 생체시계유전자의 발현을 조절함으로서 지질대사와 생체시계시스템와의 연계성을 증명하였다.
2) 2차년도 Rev-erbα/RORα이 지방산 β-oxidation에 미치는 영향과 생체시계유전자와 AMPK 경로의 상호 작용 규명: RORα에 의해 AMPK 경로의 활성화되고 생화학적으로 인산화 증대에 근거한다. Rev-erbα/RORα이 β-oxidation과 관련 유전자의 발현을 억제 또는 증대시키며, RORα 리간드에 의한 AMPK 활성화는 생체시계유전자의 발현을 증대시킨다.
3) 3차년도 Rev-erbα/RORα이 간세포 내 활성산소종 (ROS) 생성 및 Kupffer cell 활성화에 미치는 영향: 간세포에서 RORα는 전사인자로서의 직접적인 조절과 Nrf2에 의한 간접적인 조절로 SOD2와 GPx 등 항산화효소의 활성 증대를 통하여 ROS의 level을 낮추고 지질과산화를 억제한다. 또한 RORα는 간세포와 Kupffer cell에서 지방산과다 공급에 의한 염증성 싸이토카인의 발현 증진을 억제하였다. 반면 Rev-erbα는 ROS의 생성, SOD2의 발현, 염증성 싸이토카인의 발현 등에 있어서 반대 역할을 하는 것으로 판단된다.
제 2 단계: 지방간 모델에서 저분자 리간드와 genetic mutant를 이용한 Rev-erb와 ROR의 병태생리학적 역할 분석
4) 4차년도 RORα의 저분자 리간드와 Rev-erbα/RORα를 코딩하는 아데노바이러스가 high fat-induced fatty liver와 ob/ob mice의 지방간 생성에 미치는 영향: RORα의 저분자 리간드는 고지방식이 유도 지방간 개선 효과를 나타내었고, RORα은 지질대사성 간질환의 치료제로서의 가능성을 타진하였다.
5) 5차년도 Genetic mutant를 이용하여 Rev-erbα의 지질대사에서의 병태생리학적 역할 분석: Rev-erbα knockout mouse에 고지방식이 유도 지방간 모델을 정립하여 Rev-erbα의 간 내 지질대사 및 염증 반응에 관여하고 있음을 확인하였다.
연구결과의 활용계획
° 생체시계유전자 Rev-erbα/RORα와 주요 지질대사LXR/SREBP-1/FAS 경로에 의한 지질 생합성과 AMPK에 의한 지질분해의 연관성 규명 및 분자세포생물학적 측면에서의 이해로 clock genes의 생리학적 기능 조명
° Rev-erbα/RORα 커플링은 지방간, 비만, 당뇨 등 만성 대사성 질환과 수면 장애로 인한 각종 인체 질환을 타겟으로 하는 효율적 약물 작용점으로 개발될 가능성이 높음
° 핵 수용체의 새로운 생물학적 기능 및 조절 기작 규명
° 선진화된 생명의약분야의 전문가 양성
Purpose&contents
Here, we demonstrated the roles of circadian clock genes (CCGs), Rev-erbα/RORα, in the major lipid synthesis, the oxidation pathway and the reactive oxygen species production, the inflammation and the integrated control mechanisms of the circadian rhythms and lipid metabolism. Al
Purpose&contents
Here, we demonstrated the roles of circadian clock genes (CCGs), Rev-erbα/RORα, in the major lipid synthesis, the oxidation pathway and the reactive oxygen species production, the inflammation and the integrated control mechanisms of the circadian rhythms and lipid metabolism. Also, we confirmed the pathophysiologic roles of Rev-erbα/RORα by using genetic mutants and low molecular weight ligands in fatty liver model and establish the pharmacological foundation of the improvement of lipid metabolism by normalizing the activity of circadian clock genes.
Result
Step 1: Investigation of integrated control mechanisms of circadian clock genes Rev-erba/RORa and lipid metabolism at molecular level
1) The 1st year, the investigation of cross-talk between Rev-erbα/RORα and LXR/SREBP-1/FAS signal system: We identified that Rev-erbα/RORα regulated the activation of LXR pathway and analyzed the active site of LXR promoter controlled by Rev-erbα/RORα. We demonstrated the effects of Rev-erbα/RORα on the LXR trans-activation and the lipid droplets production induced by LXR activation in hepatic cells. We also examined the effects of LXR activation on the activity of the clock genes.
2) The 2nd year, the effect of Rev-erbα/RORα on the fatty acid β-oxidation: The investigation of the interaction between the circadian clock genes and the AMPK pathway. We identified that the AMPK pathway is activated by RORα and figured out linked biochemical mechanism. We demonstrated the effects of Rev-erbα/RORα on the activity of genes related to the β-oxidation and the effects of other clock genes related to the AMPK pathway.
3) The 3rd year, the effects of Rev-erbα/RORα on the ROS production in hepatic cells and the Kupffer cell activation: We demonstrated the control mechanisms of ROS homeostasis and the anti-oxidation system by Rev-erbα/RORα in the liver cells. We confirmed the effects of Rev-erbα/RORα on the Kupffer cell activation and focused on the roles of the circadian clock genes in the inflammatory reaction.
Step 2: Analysis of the pathophysiologic roles of Rev-erbα and RORα by using low molecular weight ligands and genetic mutants in fatty liver models
4) The 4th year: We identified the effects of the adenovirus coding Rev-erbα/RORα and the low molecular weight ligands on the high fat-induced fatty liver production.
5) The 5th year, analysis of the pathophysiologic roles of Rev-erbα in the lipid metabolism by using genetic mutants: We confirmed the susceptibility of the Rev-erbα knock out mice to the fatty liver.
Expected Contribution
° Focusing on the physiologic functions of clock genes by identifying the relationship between Rev-erbα/RORα and the major lipid metabolic pathways including lipid synthesis by LXR/SREBP-1/FAS pathway and the lipid oxidation by AMPK.
° Investigating the possibility of Rev-erbα/RORα clock system to be developed as the efficient pharmacologic point targeting the human diseases caused by chronic metabolic diseases such as fatty liver, obesity, and diabetes, and sleep disorders.
° Discovering the new biological function and the control mechanism of the nuclear receptors.
° Holding a dominant position in the international research competition by identifying the targets controlling clock genes and developing the verifying technique.
° Training the advanced biomedical professionals
 표
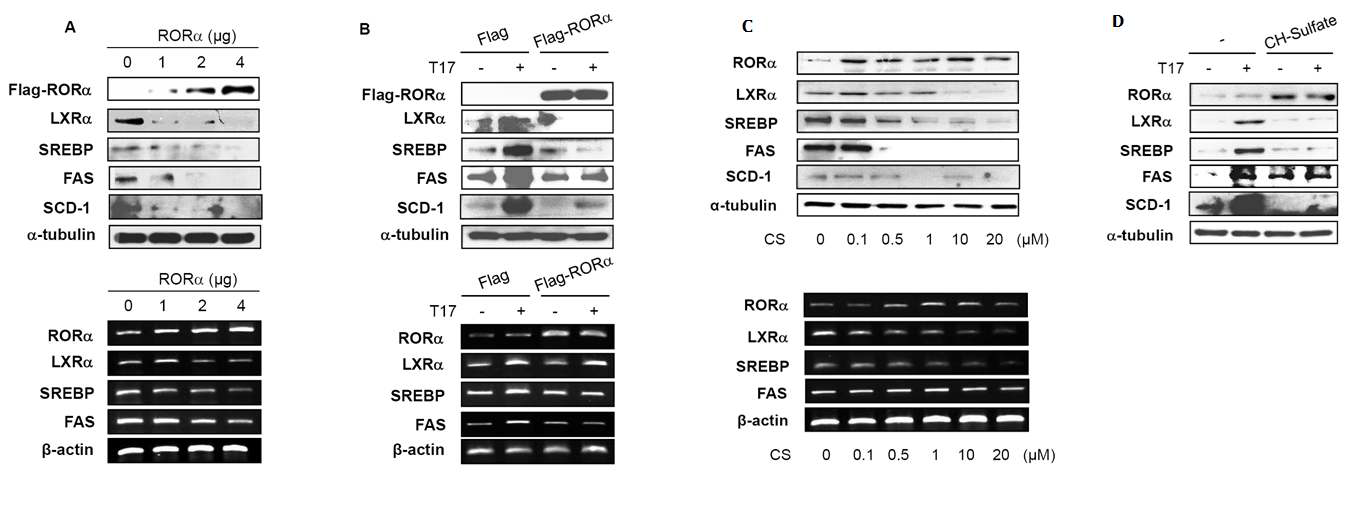
RORα가 LXRα/SREBP-1/FAS 경로의 활성화에 미치는 영향. (A) 간암 세포주 HepG2에서 RORα 과발현시 LXRα/SREBP-1/FAS의 발현 변화 (B) 간암 세포주 HepG2에서 RORα를 과발현시킨 후, TO901317 1 μM을 24 시간 처리시 LXRα/SREBP-1/FAS의 발현 변화 (C) 간암 세포주 HepG2에서 CH-Sulfate을 농도 의존적으로 처리시, LXRα/SREBP-1/FAS의 발현 변화 (D) 간암 세포주 HepG2에서 CH-Sulfate 20 μM을 24 시간 처리하여 RORα를 활성화시킨 후, TO901317 1 μM을 24시간 처리시 LXRα/SREBP-1/FAS의 단백질 발현 변화
표
RORα가 LXRα/SREBP-1/FAS 경로의 활성화에 미치는 영향. (A) 간암 세포주 HepG2에서 RORα 과발현시 LXRα/SREBP-1/FAS의 발현 변화 (B) 간암 세포주 HepG2에서 RORα를 과발현시킨 후, TO901317 1 μM을 24 시간 처리시 LXRα/SREBP-1/FAS의 발현 변화 (C) 간암 세포주 HepG2에서 CH-Sulfate을 농도 의존적으로 처리시, LXRα/SREBP-1/FAS의 발현 변화 (D) 간암 세포주 HepG2에서 CH-Sulfate 20 μM을 24 시간 처리하여 RORα를 활성화시킨 후, TO901317 1 μM을 24시간 처리시 LXRα/SREBP-1/FAS의 단백질 발현 변화
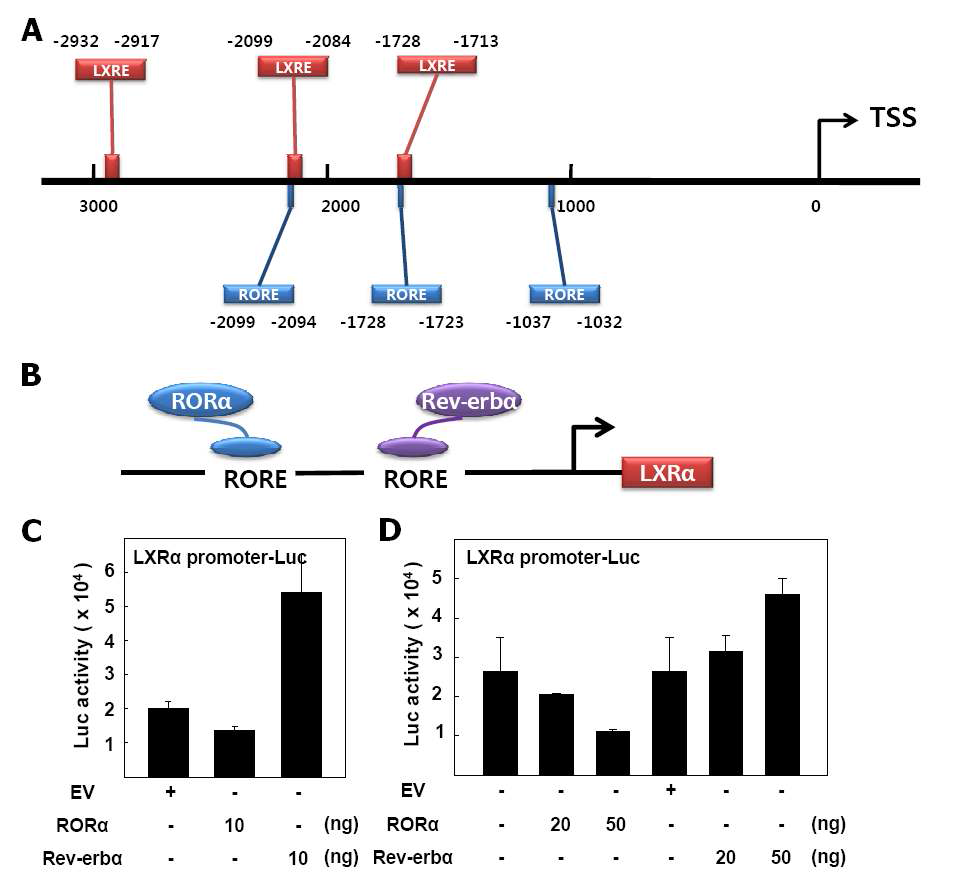 표
RORα/Rev-erbα이 LXRα Promoter에 미치는 영향 (A) LXRα promoter 분석을 통해 잠재적인 RORE (blue)와 LXRE (red) 확인. TSS: Transcription start site. (B) Schematic illustration of RORα/Rev-erbα interaction with RORE in LXRα promoter (C) CV-1 세포에서 RORα/Rev-erbα 과발현시 LXRα promoter 활성 변화 (D) 간암 세포주 HepG2에서 RORα/Rev-erbα 과발현시 LXR promoter 활성 변화
표
RORα/Rev-erbα이 LXRα Promoter에 미치는 영향 (A) LXRα promoter 분석을 통해 잠재적인 RORE (blue)와 LXRE (red) 확인. TSS: Transcription start site. (B) Schematic illustration of RORα/Rev-erbα interaction with RORE in LXRα promoter (C) CV-1 세포에서 RORα/Rev-erbα 과발현시 LXRα promoter 활성 변화 (D) 간암 세포주 HepG2에서 RORα/Rev-erbα 과발현시 LXR promoter 활성 변화
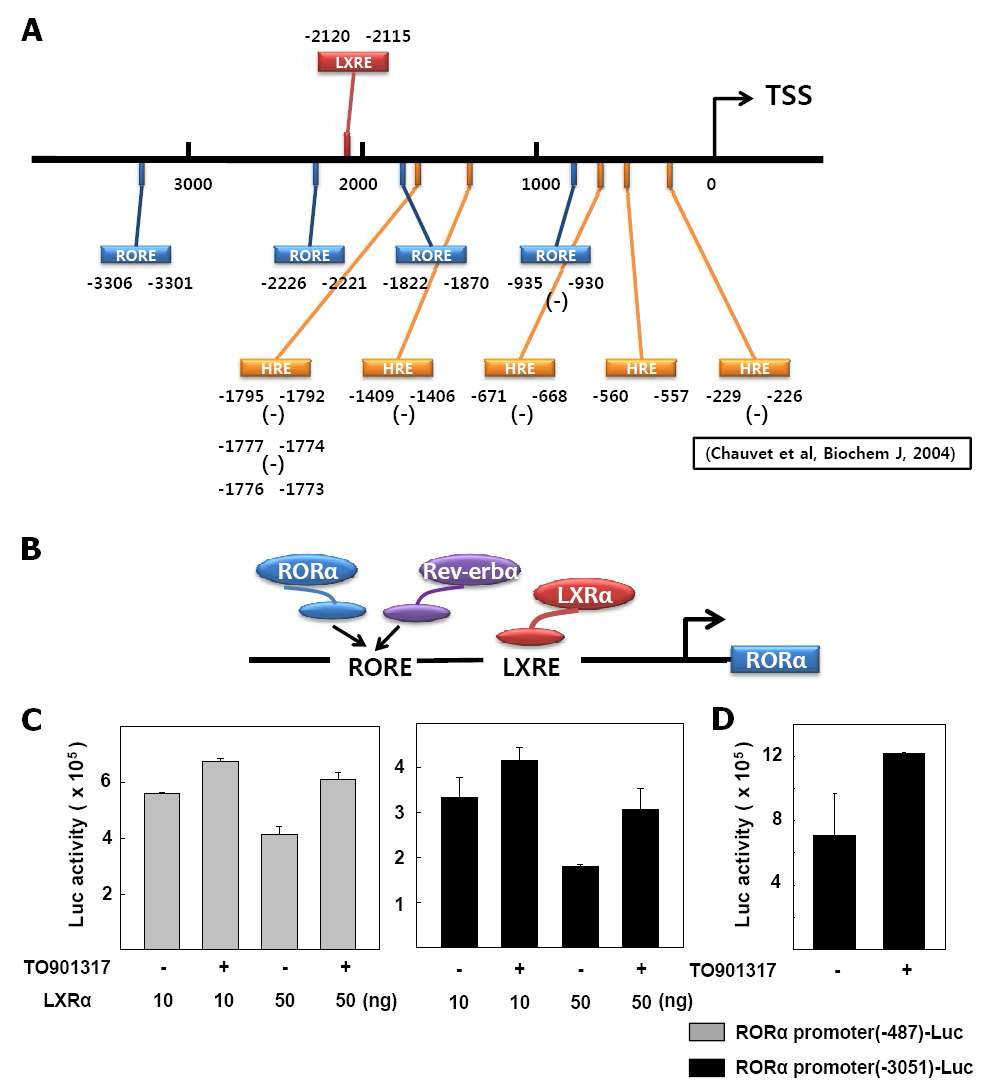 표
LXRα가 RORα Promoter에 미치는 영향 (A) RORα promoter의 sequence 분석을 통해 Putative RORE (blue), HRE (yellow), LXRE (red) 확인. TSS: Transcription start site (Chauvet et al. 2004) 참조 (B) Schematic illustration of LXRα interaction with LXRE in RORα promoter (C) CV-1 세포에서 LXRα 과발현시 RORα promoter의 활성 변화 (D) 간암 세포주 HepG2에서 TO901317 1 μM을 24 시간 처치시 RORα promoter의 활성 변화
표
LXRα가 RORα Promoter에 미치는 영향 (A) RORα promoter의 sequence 분석을 통해 Putative RORE (blue), HRE (yellow), LXRE (red) 확인. TSS: Transcription start site (Chauvet et al. 2004) 참조 (B) Schematic illustration of LXRα interaction with LXRE in RORα promoter (C) CV-1 세포에서 LXRα 과발현시 RORα promoter의 활성 변화 (D) 간암 세포주 HepG2에서 TO901317 1 μM을 24 시간 처치시 RORα promoter의 활성 변화
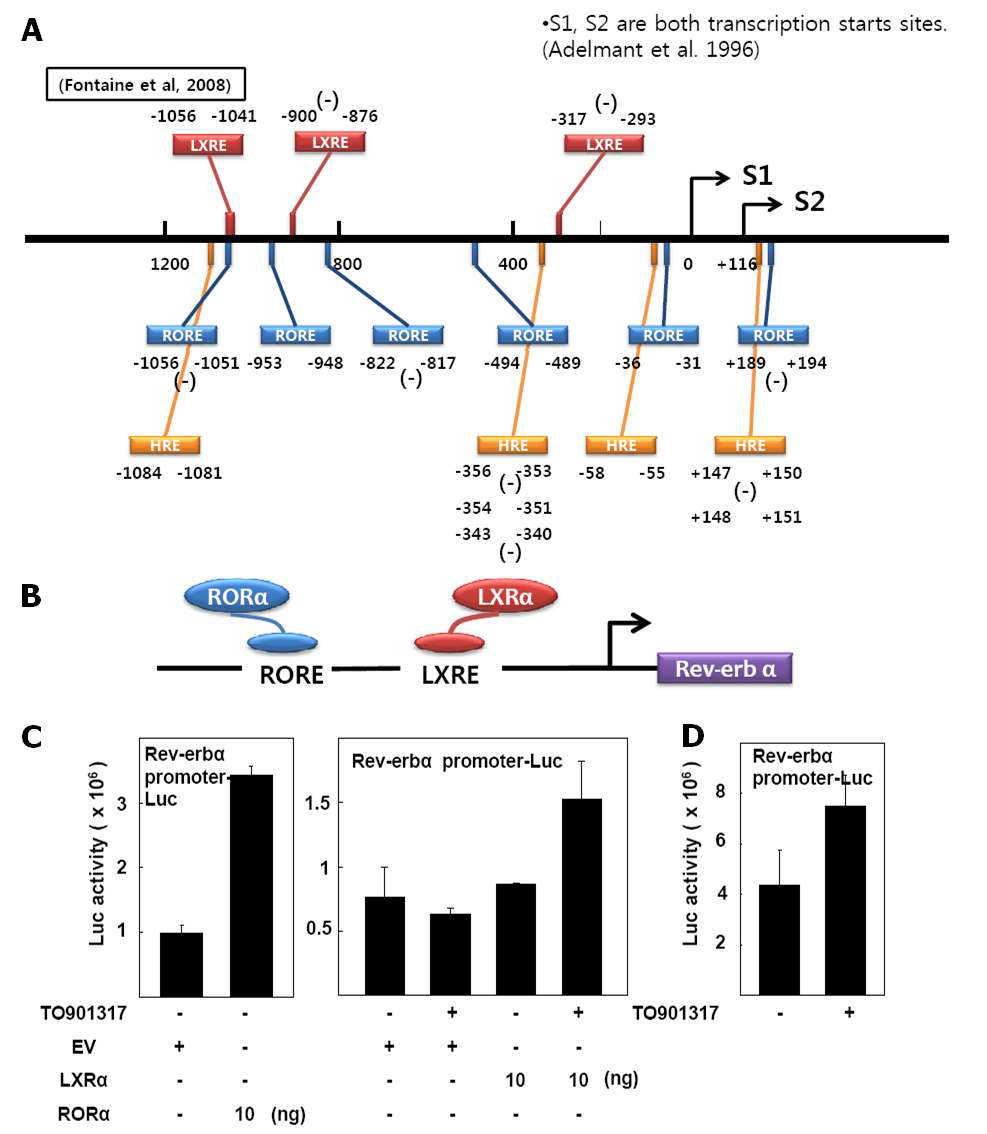 표
LXRα/RORα가 Rev-erbα Promoter에 미치는 영향 (A) Rev-erbα promoter의 시퀀스 분석을 통해 Putative RORE(blue), HRE(yellow), LXRE(red), RevRE(underline) 확인 (B) Schematic illustration of LXRα/RORα interaction with LXRE/RORE in Rev-erbα promoter (C) CV-1 세포에서 LXRα/RORα 과발현시 Rev-erbα promoter의 활성 변화 (D) HepG2에서 TO901317 1 μM을 24 시간 처리시 Rev-erbα promoter의 활성 변화
표
LXRα/RORα가 Rev-erbα Promoter에 미치는 영향 (A) Rev-erbα promoter의 시퀀스 분석을 통해 Putative RORE(blue), HRE(yellow), LXRE(red), RevRE(underline) 확인 (B) Schematic illustration of LXRα/RORα interaction with LXRE/RORE in Rev-erbα promoter (C) CV-1 세포에서 LXRα/RORα 과발현시 Rev-erbα promoter의 활성 변화 (D) HepG2에서 TO901317 1 μM을 24 시간 처리시 Rev-erbα promoter의 활성 변화
 표
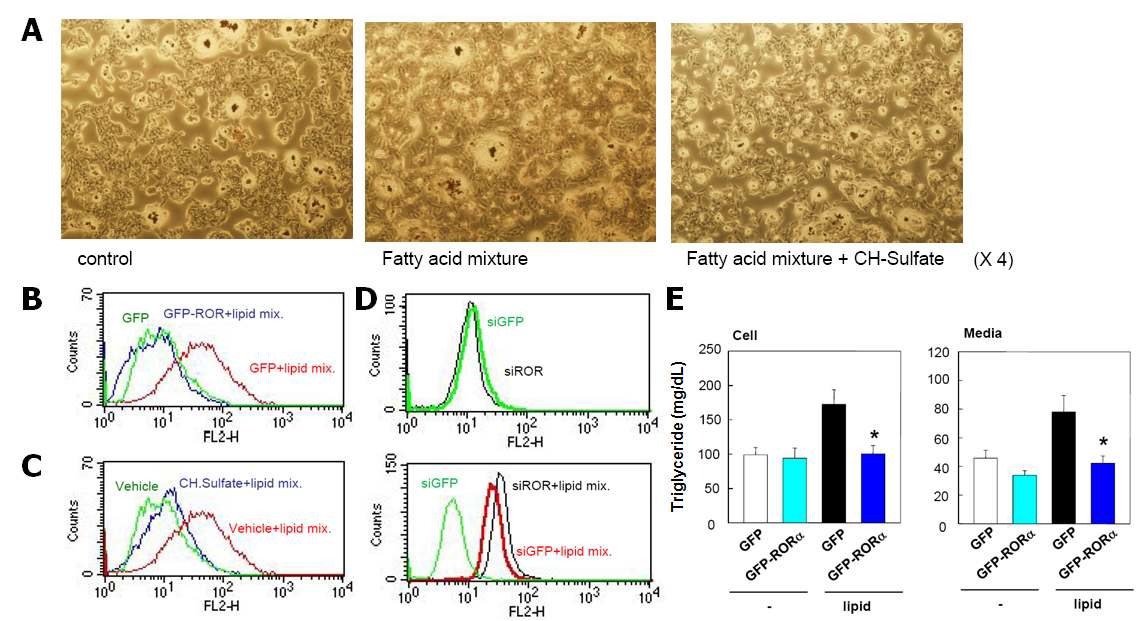
Fatty acid mixture의 활성화로 간세포에서 유도되는 lipid droplets 생성에 RORα가 미치는 영향. (A) HepG2에서 fatty acid mixture 0.5 %를 처리하여 lipid droplets을 형성시킨 후, CH-Sulfate를 72 시간 처리시 lipid 생성 변화 (B) HepG2에서 RORα virus infection에 의한 과발현시 lipid 생성 변화 (C) CH-Sulfate 처리시 lipid 생성 변화 (D) si-RORα transfection 시킨 후 lipid 생성 변화 (E) 간 세포주 Chang에서 fatty acid mixture 0.5 %와 RORα virus 처리 72 시간 후, triglyceride의 생성 변화
표
Fatty acid mixture의 활성화로 간세포에서 유도되는 lipid droplets 생성에 RORα가 미치는 영향. (A) HepG2에서 fatty acid mixture 0.5 %를 처리하여 lipid droplets을 형성시킨 후, CH-Sulfate를 72 시간 처리시 lipid 생성 변화 (B) HepG2에서 RORα virus infection에 의한 과발현시 lipid 생성 변화 (C) CH-Sulfate 처리시 lipid 생성 변화 (D) si-RORα transfection 시킨 후 lipid 생성 변화 (E) 간 세포주 Chang에서 fatty acid mixture 0.5 %와 RORα virus 처리 72 시간 후, triglyceride의 생성 변화
 표
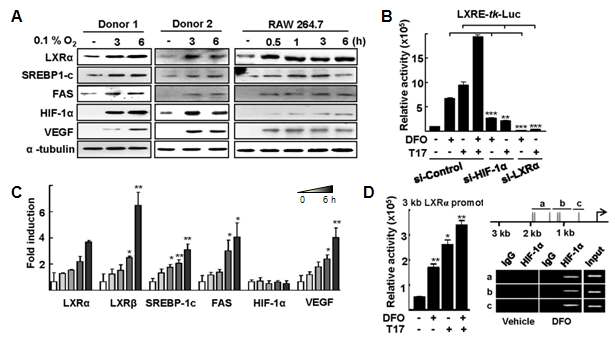
저산소에 의해 유도되는 지질 관련 유전자 (A) Human primary macrophages와 Raw 264.7 세포의 시간에 따른 저산소 처리 후 단백질 발현 확인 (B) Raw 264.7 세포에 si-RNA와 LXRE-luc. 과발현 후 LXRE reporter 유전자 분석 (C) Raw 264.7 세포에 저산소 처리 후 real-time PCR로 mRNA level 분석 (D) LXRa 프로모터 reporter를 발현시킨 후 저산소 12 시간 또는 LXRa ligand (TO901317) 처리 후 reporter 유전자 분석 (왼쪽). 표시된 DNA 영역에 대하여 ChIP 분석
표
저산소에 의해 유도되는 지질 관련 유전자 (A) Human primary macrophages와 Raw 264.7 세포의 시간에 따른 저산소 처리 후 단백질 발현 확인 (B) Raw 264.7 세포에 si-RNA와 LXRE-luc. 과발현 후 LXRE reporter 유전자 분석 (C) Raw 264.7 세포에 저산소 처리 후 real-time PCR로 mRNA level 분석 (D) LXRa 프로모터 reporter를 발현시킨 후 저산소 12 시간 또는 LXRa ligand (TO901317) 처리 후 reporter 유전자 분석 (왼쪽). 표시된 DNA 영역에 대하여 ChIP 분석
 표
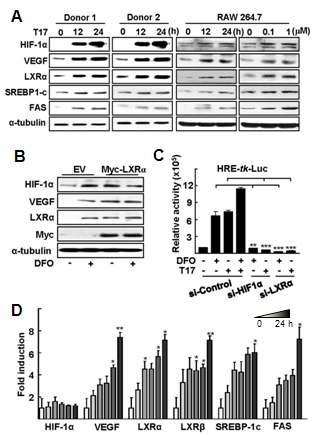
LXRα의 활성화에 의한 HIF-1α의 활성 증가 (A) 사람의 혈액으로부터 분리된 macrophages와 Raw 264.7 세포의 시간 또는 농도에 따른 LXRα 리간드 TO901317 처리 후, 단백질 발현 확인(B) Raw 264.7 세포에 LXRα 과발현 후, 단백질 발현 확인(C) Raw 264.7 세포에 12시간 저산소와 24시간 LXRα 리간드 TO901317 처리 후, HRE-luc reporter 유전자 발현 분석 (D) Raw 264.7 세포에 TO901317 처리 후, real-time PCR로 mRNA level을 분석
표
LXRα의 활성화에 의한 HIF-1α의 활성 증가 (A) 사람의 혈액으로부터 분리된 macrophages와 Raw 264.7 세포의 시간 또는 농도에 따른 LXRα 리간드 TO901317 처리 후, 단백질 발현 확인(B) Raw 264.7 세포에 LXRα 과발현 후, 단백질 발현 확인(C) Raw 264.7 세포에 12시간 저산소와 24시간 LXRα 리간드 TO901317 처리 후, HRE-luc reporter 유전자 발현 분석 (D) Raw 264.7 세포에 TO901317 처리 후, real-time PCR로 mRNA level을 분석
 표
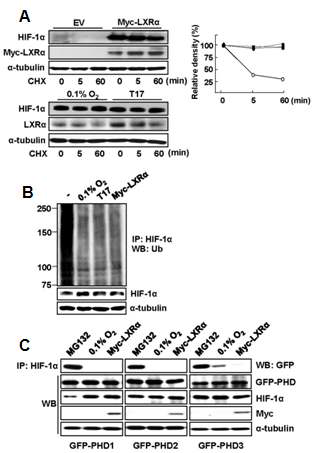
LXRα에 의한 HIF-1α의 안정화(A) Raw 264.7 세포에 LXRα 과발현 후 cyclohexamide 10 μM을 시간에 따라 처리 후, 단백질 발현 확인 (왼쪽) 단백질 band를 정량화하여 control과 대비하여 그래프로 나타냄 (오른쪽)(B) LXRα 과발현 또는 저산소, TO901317 처리 후, 면역침강과 western blot을 통하여 단백질의 ubiquitination 정도 확인(C) NIH3T3 세포에 지칭한 벡터를 각각 과발현 또는 저산소, 10 μM MG132를 처리한 후 면역침강과 western blot 방법으로 HIF-1α 와 PHD의 단백질 상호작용 분석
표
LXRα에 의한 HIF-1α의 안정화(A) Raw 264.7 세포에 LXRα 과발현 후 cyclohexamide 10 μM을 시간에 따라 처리 후, 단백질 발현 확인 (왼쪽) 단백질 band를 정량화하여 control과 대비하여 그래프로 나타냄 (오른쪽)(B) LXRα 과발현 또는 저산소, TO901317 처리 후, 면역침강과 western blot을 통하여 단백질의 ubiquitination 정도 확인(C) NIH3T3 세포에 지칭한 벡터를 각각 과발현 또는 저산소, 10 μM MG132를 처리한 후 면역침강과 western blot 방법으로 HIF-1α 와 PHD의 단백질 상호작용 분석
 표
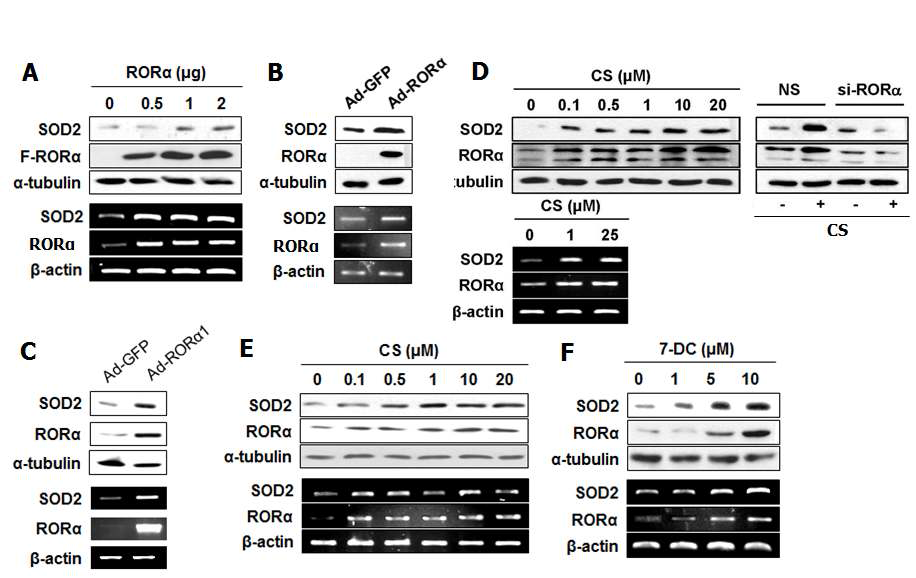
RORα에 의한 SOD2의 조절 (A) HepG2에서 RORα 과발현시 SOD2 발현 변화 (B) HepG2에서 RORα virus infection 후, SOD2 발현 변화 (C) Primary hepatocyte에서 RORα virus infection 후, SOD2 발현 변화 (D) HepG2에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리 시, SOD2 발현 변화 / si-RORα를 transfection 시킨 후, CS 25 μΜ 처리시, SOD2 단백질 발현 변화 (E) Primary hepatocyte에서 RORα 리간드 CS와 7-DC 처리시 SOD2 발현 변화
표
RORα에 의한 SOD2의 조절 (A) HepG2에서 RORα 과발현시 SOD2 발현 변화 (B) HepG2에서 RORα virus infection 후, SOD2 발현 변화 (C) Primary hepatocyte에서 RORα virus infection 후, SOD2 발현 변화 (D) HepG2에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리 시, SOD2 발현 변화 / si-RORα를 transfection 시킨 후, CS 25 μΜ 처리시, SOD2 단백질 발현 변화 (E) Primary hepatocyte에서 RORα 리간드 CS와 7-DC 처리시 SOD2 발현 변화
 표
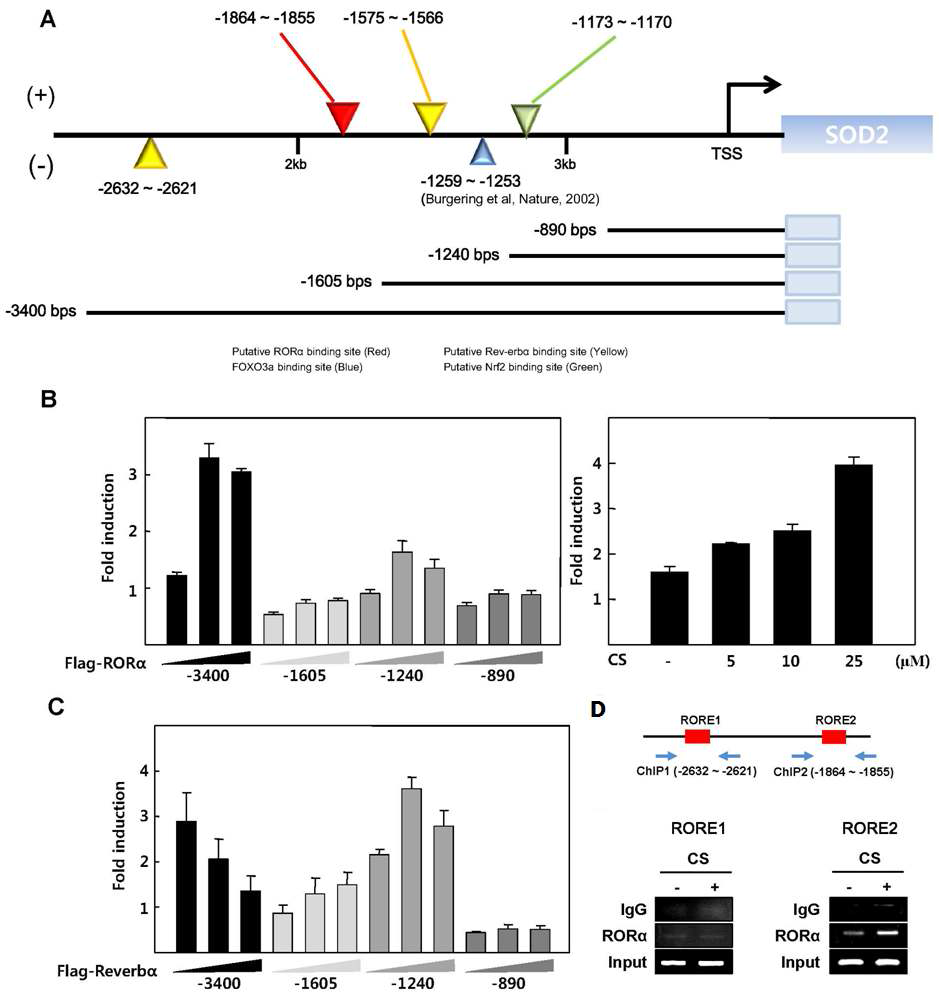
RORα에 의한 SOD2 promoter의 활성 변화 (A) SOD2 promoter의 sequence분석을 통한 Putative RORE (red), RevRE (yellow), FOXO3a binding site (blue), ARE (green)와 현재 갖고 있는 4개의 길이별 SOD2 promoter (B) RORα 과발현 시 SOD2-promoter 길이별 활성 변화와 Chang cell line에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리시, SOD2-promoter 3.4kb의 활성 변화(C) Rev-erbα 과발현시 SOD2-promoter 길이별 활성 변화 (D) SOD2 promoter의 putative RORα binding site sequence 및 HepG2에서 CS 처리 시 RORα binding 증가 확인
표
RORα에 의한 SOD2 promoter의 활성 변화 (A) SOD2 promoter의 sequence분석을 통한 Putative RORE (red), RevRE (yellow), FOXO3a binding site (blue), ARE (green)와 현재 갖고 있는 4개의 길이별 SOD2 promoter (B) RORα 과발현 시 SOD2-promoter 길이별 활성 변화와 Chang cell line에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리시, SOD2-promoter 3.4kb의 활성 변화(C) Rev-erbα 과발현시 SOD2-promoter 길이별 활성 변화 (D) SOD2 promoter의 putative RORα binding site sequence 및 HepG2에서 CS 처리 시 RORα binding 증가 확인
 표
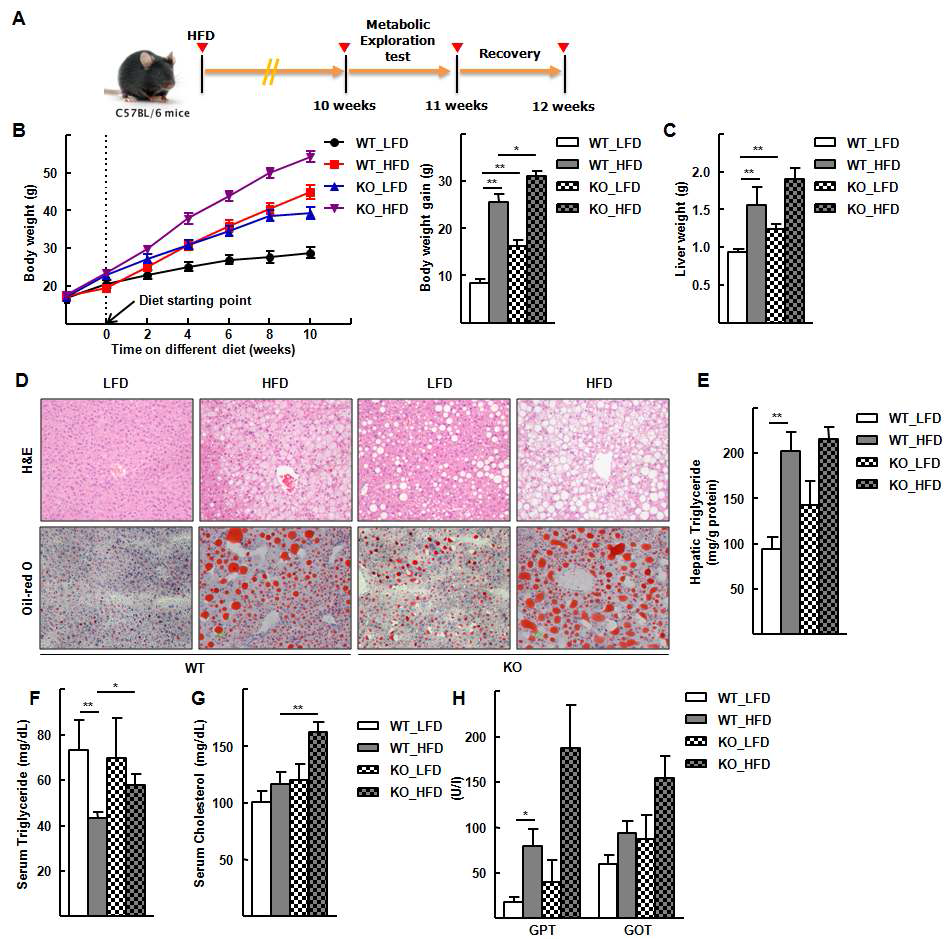
Rev-erbα knockout mouse 지방간 유도 모델에서의 지질합성. (A) 고지방식이 (High fat diet, HFD)에 따른 지방간 유도 모델의 정립. (B) 2주 간격의 체중 측정. 저지방식이 (Low fat diet, LFD)에 대비되어 WT와 KO mouse 모두에서 체중 증가됨. (C) genotype과 식이에 따른 간 무게 변화 (D) genotype과 식이에 따른 간 조직 조직면역염색 분석. H&E, Oil-red O 염색. (E) 간 조직 내의 중성 지방 변화 (F), (G) 혈청 내의 중성지방과 콜레스테롤 변화
표
Rev-erbα knockout mouse 지방간 유도 모델에서의 지질합성. (A) 고지방식이 (High fat diet, HFD)에 따른 지방간 유도 모델의 정립. (B) 2주 간격의 체중 측정. 저지방식이 (Low fat diet, LFD)에 대비되어 WT와 KO mouse 모두에서 체중 증가됨. (C) genotype과 식이에 따른 간 무게 변화 (D) genotype과 식이에 따른 간 조직 조직면역염색 분석. H&E, Oil-red O 염색. (E) 간 조직 내의 중성 지방 변화 (F), (G) 혈청 내의 중성지방과 콜레스테롤 변화
 표
RORα가 LXRα/SREBP-1/FAS 경로의 활성화에 미치는 영향. (A) 간암 세포주 HepG2에서 RORα 과발현시 LXRα/SREBP-1/FAS의 발현 변화 (B) 간암 세포주 HepG2에서 RORα를 과발현시킨 후, TO901317 1 μM을 24 시간 처리시 LXRα/SREBP-1/FAS의 발현 변화 (C) 간암 세포주 HepG2에서 CH-Sulfate을 농도 의존적으로 처리시, LXRα/SREBP-1/FAS의 발현 변화 (D) 간암 세포주 HepG2에서 CH-Sulfate 20 μM을 24 시간 처리하여 RORα를 활성화시킨 후, TO901317 1 μM을 24시간 처리시 LXRα/SREBP-1/FAS의 단백질 발현 변화
표
RORα가 LXRα/SREBP-1/FAS 경로의 활성화에 미치는 영향. (A) 간암 세포주 HepG2에서 RORα 과발현시 LXRα/SREBP-1/FAS의 발현 변화 (B) 간암 세포주 HepG2에서 RORα를 과발현시킨 후, TO901317 1 μM을 24 시간 처리시 LXRα/SREBP-1/FAS의 발현 변화 (C) 간암 세포주 HepG2에서 CH-Sulfate을 농도 의존적으로 처리시, LXRα/SREBP-1/FAS의 발현 변화 (D) 간암 세포주 HepG2에서 CH-Sulfate 20 μM을 24 시간 처리하여 RORα를 활성화시킨 후, TO901317 1 μM을 24시간 처리시 LXRα/SREBP-1/FAS의 단백질 발현 변화
 표
RORα/Rev-erbα이 LXRα Promoter에 미치는 영향 (A) LXRα promoter 분석을 통해 잠재적인 RORE (blue)와 LXRE (red) 확인. TSS: Transcription start site. (B) Schematic illustration of RORα/Rev-erbα interaction with RORE in LXRα promoter (C) CV-1 세포에서 RORα/Rev-erbα 과발현시 LXRα promoter 활성 변화 (D) 간암 세포주 HepG2에서 RORα/Rev-erbα 과발현시 LXR promoter 활성 변화
표
RORα/Rev-erbα이 LXRα Promoter에 미치는 영향 (A) LXRα promoter 분석을 통해 잠재적인 RORE (blue)와 LXRE (red) 확인. TSS: Transcription start site. (B) Schematic illustration of RORα/Rev-erbα interaction with RORE in LXRα promoter (C) CV-1 세포에서 RORα/Rev-erbα 과발현시 LXRα promoter 활성 변화 (D) 간암 세포주 HepG2에서 RORα/Rev-erbα 과발현시 LXR promoter 활성 변화
 표
LXRα가 RORα Promoter에 미치는 영향 (A) RORα promoter의 sequence 분석을 통해 Putative RORE (blue), HRE (yellow), LXRE (red) 확인. TSS: Transcription start site (Chauvet et al. 2004) 참조 (B) Schematic illustration of LXRα interaction with LXRE in RORα promoter (C) CV-1 세포에서 LXRα 과발현시 RORα promoter의 활성 변화 (D) 간암 세포주 HepG2에서 TO901317 1 μM을 24 시간 처치시 RORα promoter의 활성 변화
표
LXRα가 RORα Promoter에 미치는 영향 (A) RORα promoter의 sequence 분석을 통해 Putative RORE (blue), HRE (yellow), LXRE (red) 확인. TSS: Transcription start site (Chauvet et al. 2004) 참조 (B) Schematic illustration of LXRα interaction with LXRE in RORα promoter (C) CV-1 세포에서 LXRα 과발현시 RORα promoter의 활성 변화 (D) 간암 세포주 HepG2에서 TO901317 1 μM을 24 시간 처치시 RORα promoter의 활성 변화
 표
LXRα/RORα가 Rev-erbα Promoter에 미치는 영향 (A) Rev-erbα promoter의 시퀀스 분석을 통해 Putative RORE(blue), HRE(yellow), LXRE(red), RevRE(underline) 확인 (B) Schematic illustration of LXRα/RORα interaction with LXRE/RORE in Rev-erbα promoter (C) CV-1 세포에서 LXRα/RORα 과발현시 Rev-erbα promoter의 활성 변화 (D) HepG2에서 TO901317 1 μM을 24 시간 처리시 Rev-erbα promoter의 활성 변화
표
LXRα/RORα가 Rev-erbα Promoter에 미치는 영향 (A) Rev-erbα promoter의 시퀀스 분석을 통해 Putative RORE(blue), HRE(yellow), LXRE(red), RevRE(underline) 확인 (B) Schematic illustration of LXRα/RORα interaction with LXRE/RORE in Rev-erbα promoter (C) CV-1 세포에서 LXRα/RORα 과발현시 Rev-erbα promoter의 활성 변화 (D) HepG2에서 TO901317 1 μM을 24 시간 처리시 Rev-erbα promoter의 활성 변화
 표
Fatty acid mixture의 활성화로 간세포에서 유도되는 lipid droplets 생성에 RORα가 미치는 영향. (A) HepG2에서 fatty acid mixture 0.5 %를 처리하여 lipid droplets을 형성시킨 후, CH-Sulfate를 72 시간 처리시 lipid 생성 변화 (B) HepG2에서 RORα virus infection에 의한 과발현시 lipid 생성 변화 (C) CH-Sulfate 처리시 lipid 생성 변화 (D) si-RORα transfection 시킨 후 lipid 생성 변화 (E) 간 세포주 Chang에서 fatty acid mixture 0.5 %와 RORα virus 처리 72 시간 후, triglyceride의 생성 변화
표
Fatty acid mixture의 활성화로 간세포에서 유도되는 lipid droplets 생성에 RORα가 미치는 영향. (A) HepG2에서 fatty acid mixture 0.5 %를 처리하여 lipid droplets을 형성시킨 후, CH-Sulfate를 72 시간 처리시 lipid 생성 변화 (B) HepG2에서 RORα virus infection에 의한 과발현시 lipid 생성 변화 (C) CH-Sulfate 처리시 lipid 생성 변화 (D) si-RORα transfection 시킨 후 lipid 생성 변화 (E) 간 세포주 Chang에서 fatty acid mixture 0.5 %와 RORα virus 처리 72 시간 후, triglyceride의 생성 변화
 표
저산소에 의해 유도되는 지질 관련 유전자 (A) Human primary macrophages와 Raw 264.7 세포의 시간에 따른 저산소 처리 후 단백질 발현 확인 (B) Raw 264.7 세포에 si-RNA와 LXRE-luc. 과발현 후 LXRE reporter 유전자 분석 (C) Raw 264.7 세포에 저산소 처리 후 real-time PCR로 mRNA level 분석 (D) LXRa 프로모터 reporter를 발현시킨 후 저산소 12 시간 또는 LXRa ligand (TO901317) 처리 후 reporter 유전자 분석 (왼쪽). 표시된 DNA 영역에 대하여 ChIP 분석
표
저산소에 의해 유도되는 지질 관련 유전자 (A) Human primary macrophages와 Raw 264.7 세포의 시간에 따른 저산소 처리 후 단백질 발현 확인 (B) Raw 264.7 세포에 si-RNA와 LXRE-luc. 과발현 후 LXRE reporter 유전자 분석 (C) Raw 264.7 세포에 저산소 처리 후 real-time PCR로 mRNA level 분석 (D) LXRa 프로모터 reporter를 발현시킨 후 저산소 12 시간 또는 LXRa ligand (TO901317) 처리 후 reporter 유전자 분석 (왼쪽). 표시된 DNA 영역에 대하여 ChIP 분석
 표
LXRα의 활성화에 의한 HIF-1α의 활성 증가 (A) 사람의 혈액으로부터 분리된 macrophages와 Raw 264.7 세포의 시간 또는 농도에 따른 LXRα 리간드 TO901317 처리 후, 단백질 발현 확인(B) Raw 264.7 세포에 LXRα 과발현 후, 단백질 발현 확인(C) Raw 264.7 세포에 12시간 저산소와 24시간 LXRα 리간드 TO901317 처리 후, HRE-luc reporter 유전자 발현 분석 (D) Raw 264.7 세포에 TO901317 처리 후, real-time PCR로 mRNA level을 분석
표
LXRα의 활성화에 의한 HIF-1α의 활성 증가 (A) 사람의 혈액으로부터 분리된 macrophages와 Raw 264.7 세포의 시간 또는 농도에 따른 LXRα 리간드 TO901317 처리 후, 단백질 발현 확인(B) Raw 264.7 세포에 LXRα 과발현 후, 단백질 발현 확인(C) Raw 264.7 세포에 12시간 저산소와 24시간 LXRα 리간드 TO901317 처리 후, HRE-luc reporter 유전자 발현 분석 (D) Raw 264.7 세포에 TO901317 처리 후, real-time PCR로 mRNA level을 분석
 표
LXRα에 의한 HIF-1α의 안정화(A) Raw 264.7 세포에 LXRα 과발현 후 cyclohexamide 10 μM을 시간에 따라 처리 후, 단백질 발현 확인 (왼쪽) 단백질 band를 정량화하여 control과 대비하여 그래프로 나타냄 (오른쪽)(B) LXRα 과발현 또는 저산소, TO901317 처리 후, 면역침강과 western blot을 통하여 단백질의 ubiquitination 정도 확인(C) NIH3T3 세포에 지칭한 벡터를 각각 과발현 또는 저산소, 10 μM MG132를 처리한 후 면역침강과 western blot 방법으로 HIF-1α 와 PHD의 단백질 상호작용 분석
표
LXRα에 의한 HIF-1α의 안정화(A) Raw 264.7 세포에 LXRα 과발현 후 cyclohexamide 10 μM을 시간에 따라 처리 후, 단백질 발현 확인 (왼쪽) 단백질 band를 정량화하여 control과 대비하여 그래프로 나타냄 (오른쪽)(B) LXRα 과발현 또는 저산소, TO901317 처리 후, 면역침강과 western blot을 통하여 단백질의 ubiquitination 정도 확인(C) NIH3T3 세포에 지칭한 벡터를 각각 과발현 또는 저산소, 10 μM MG132를 처리한 후 면역침강과 western blot 방법으로 HIF-1α 와 PHD의 단백질 상호작용 분석
 표
RORα에 의한 SOD2의 조절 (A) HepG2에서 RORα 과발현시 SOD2 발현 변화 (B) HepG2에서 RORα virus infection 후, SOD2 발현 변화 (C) Primary hepatocyte에서 RORα virus infection 후, SOD2 발현 변화 (D) HepG2에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리 시, SOD2 발현 변화 / si-RORα를 transfection 시킨 후, CS 25 μΜ 처리시, SOD2 단백질 발현 변화 (E) Primary hepatocyte에서 RORα 리간드 CS와 7-DC 처리시 SOD2 발현 변화
표
RORα에 의한 SOD2의 조절 (A) HepG2에서 RORα 과발현시 SOD2 발현 변화 (B) HepG2에서 RORα virus infection 후, SOD2 발현 변화 (C) Primary hepatocyte에서 RORα virus infection 후, SOD2 발현 변화 (D) HepG2에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리 시, SOD2 발현 변화 / si-RORα를 transfection 시킨 후, CS 25 μΜ 처리시, SOD2 단백질 발현 변화 (E) Primary hepatocyte에서 RORα 리간드 CS와 7-DC 처리시 SOD2 발현 변화
 표
RORα에 의한 SOD2 promoter의 활성 변화 (A) SOD2 promoter의 sequence분석을 통한 Putative RORE (red), RevRE (yellow), FOXO3a binding site (blue), ARE (green)와 현재 갖고 있는 4개의 길이별 SOD2 promoter (B) RORα 과발현 시 SOD2-promoter 길이별 활성 변화와 Chang cell line에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리시, SOD2-promoter 3.4kb의 활성 변화(C) Rev-erbα 과발현시 SOD2-promoter 길이별 활성 변화 (D) SOD2 promoter의 putative RORα binding site sequence 및 HepG2에서 CS 처리 시 RORα binding 증가 확인
표
RORα에 의한 SOD2 promoter의 활성 변화 (A) SOD2 promoter의 sequence분석을 통한 Putative RORE (red), RevRE (yellow), FOXO3a binding site (blue), ARE (green)와 현재 갖고 있는 4개의 길이별 SOD2 promoter (B) RORα 과발현 시 SOD2-promoter 길이별 활성 변화와 Chang cell line에서 RORα 리간드인 CS를 농도 의존적으로 24 시간 처리시, SOD2-promoter 3.4kb의 활성 변화(C) Rev-erbα 과발현시 SOD2-promoter 길이별 활성 변화 (D) SOD2 promoter의 putative RORα binding site sequence 및 HepG2에서 CS 처리 시 RORα binding 증가 확인
 표
Rev-erbα knockout mouse 지방간 유도 모델에서의 지질합성. (A) 고지방식이 (High fat diet, HFD)에 따른 지방간 유도 모델의 정립. (B) 2주 간격의 체중 측정. 저지방식이 (Low fat diet, LFD)에 대비되어 WT와 KO mouse 모두에서 체중 증가됨. (C) genotype과 식이에 따른 간 무게 변화 (D) genotype과 식이에 따른 간 조직 조직면역염색 분석. H&E, Oil-red O 염색. (E) 간 조직 내의 중성 지방 변화 (F), (G) 혈청 내의 중성지방과 콜레스테롤 변화
표
Rev-erbα knockout mouse 지방간 유도 모델에서의 지질합성. (A) 고지방식이 (High fat diet, HFD)에 따른 지방간 유도 모델의 정립. (B) 2주 간격의 체중 측정. 저지방식이 (Low fat diet, LFD)에 대비되어 WT와 KO mouse 모두에서 체중 증가됨. (C) genotype과 식이에 따른 간 무게 변화 (D) genotype과 식이에 따른 간 조직 조직면역염색 분석. H&E, Oil-red O 염색. (E) 간 조직 내의 중성 지방 변화 (F), (G) 혈청 내의 중성지방과 콜레스테롤 변화
| 과제명(ProjectTitle) : | - |
|---|---|
| 연구책임자(Manager) : | - |
| 과제기간(DetailSeriesProject) : | - |
| 총연구비 (DetailSeriesProject) : | - |
| 키워드(keyword) : | - |
| 과제수행기간(LeadAgency) : | - |
| 연구목표(Goal) : | - |
| 연구내용(Abstract) : | - |
| 기대효과(Effect) : | - |
Copyright KISTI. All Rights Reserved.

※ AI-Helper는 부적절한 답변을 할 수 있습니다.