최소 단어 이상 선택하여야 합니다.
최대 10 단어까지만 선택 가능합니다.
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
NTIS 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
DataON 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Edison 바로가기
다음과 같은 기능을 한번의 로그인으로 사용 할 수 있습니다.
Kafe 바로가기
| 주관연구기관 | 부산대학교 산학협력단 Busan National University |
|---|---|
| 연구책임자 | 김민수 |
| 참여연구자 | 황성주 , 정성훈 , 신상문 , 최두형 , 하은솔 , 국도훈 , 하동현 , 이지연 , 현상민 , 곽상원 , 유나래 , 임대곤 , 정준혁 , 박성민 , 신동석 |
| 보고서유형 | 최종보고서 |
| 발행국가 | 대한민국 |
| 언어 | 한국어 |
| 발행년월 | 2016-11 |
| 과제시작연도 | 2016 |
| 주관부처 | 식품의약품안전처 Ministry of Food and Drug Safety |
| 등록번호 | TRKO201700017741 |
| 과제고유번호 | 1475008996 |
| 사업명 | 의약품등안전관리 |
| DB 구축일자 | 2017-12-02 |
| 키워드 | 설계기반품질.위해평가.공정관리.디자인스페이스.Quality by Design.Risk Assessment.Process Control.Design Space. |
| DOI | https://doi.org/10.23000/TRKO201700017741 |
의약품 품질에 대한 개념이 변화되어 설계기반품질(Quality by Design, QbD)과 관련된 가이드라인이 미국, EU, WHO, ICH 등에서 발표되고 있으며, 이와 관련하여 선진국을 중심으로 새로운 품질규제 방향을 제시하고 관련 심사, 정책 수립 등에 반영되고 있다. 세계적 제약 회사들은 이러한 규제 및 생산기술의 변화에 대응하기 위하여 자체적으로 가이드라인을 수립하고 적극적인 조치를 강구하고 있는 사례들이 발표되고 있다. 국내에서도 QbD 개념에 대한 이해도가 향상되었으나 이를 실질적으로 허가에 반영한 QbD 제도 도입을
의약품 품질에 대한 개념이 변화되어 설계기반품질(Quality by Design, QbD)과 관련된 가이드라인이 미국, EU, WHO, ICH 등에서 발표되고 있으며, 이와 관련하여 선진국을 중심으로 새로운 품질규제 방향을 제시하고 관련 심사, 정책 수립 등에 반영되고 있다. 세계적 제약 회사들은 이러한 규제 및 생산기술의 변화에 대응하기 위하여 자체적으로 가이드라인을 수립하고 적극적인 조치를 강구하고 있는 사례들이 발표되고 있다. 국내에서도 QbD 개념에 대한 이해도가 향상되었으나 이를 실질적으로 허가에 반영한 QbD 제도 도입을 위해서는 표준화된 QbD 실행절차 마련이 시급하며, 특히 QbD 핵심요소인 위해평가 및 디자인스페이스의 자료제출 예시 및 이를 과학적인 근거에 따라 체계적으로 평가할 수 있는 평가방법 마련이 시급히 요구된다. 본 연구에서는 위해관리 기반 의약품 품질평가의 규제조화 및 우수한 품질이 확보된 의약품 공급을 위한 QbD 제도 도입에 필요한 기반구축을 위해 관련핵심요소인 위해 평가와 디자인스페이스의 평가방법 마련 및 최신 품질심사 평가방법 연구, QbD 제도 도입을 위한 위해평가기술 및 평가방법 연구, 통계적 의미와 해석을 포함한 QbD 시스템 평가 방안 마련연구 및 최신 품질심사 평가방법 연구를 수행하였다. 본 과제를 통하여 마련된 QbD 핵심요소인 위해평가와 디자인스페이스 자료제출 예시 및 평가방법은 심사자 전문성 강화 및 제약업계 의약품 개발 및 해외수출에 지원뿐만 아니라 QbD 제도 도입을 위한 기초자료 및 ‘ 의약품 우수심사기준업무수행편람’개정 등에 활용될 것으로 기대된다.
( 출처 : 요약문 6p )
In this study, we analyzed the establishment procedure and regulatory approaches of risk assessment and design space with a current status of QbD–based applications in FDA, EMA, PMDA, etc. Two examples of risk assessment procedure for reviewers and scientists were provided by using descriptive risk
In this study, we analyzed the establishment procedure and regulatory approaches of risk assessment and design space with a current status of QbD–based applications in FDA, EMA, PMDA, etc. Two examples of risk assessment procedure for reviewers and scientists were provided by using descriptive risk assessment method and statistical risk assessment method including quality function deployment (QFD) and fail mode effect analysis (FMEA). In addition, examples of design space for reviewers and scientists were provided including statistical data analysis based on Design of Experiment (DoE) methods. Furthermore, we analyzed the establishment procedure and regulatory approaches of process analytical technology (PAT) for quality control and evaluation using Near-infrared spectroscopy, Raman spectroscopy, Focused Beam Reflectance Measurement (FBRM). From this study, we suggest the evaluation guide for reviewer with representative examples of risk assessment, design space, and PAT in pharmaceutical industry. It can be expected to use as a QbD-guided toolbox of risk assessment and design space to understand and implement QbD system in pharmaceutical process.
( 출처 : SUMMARY 8p )
 표
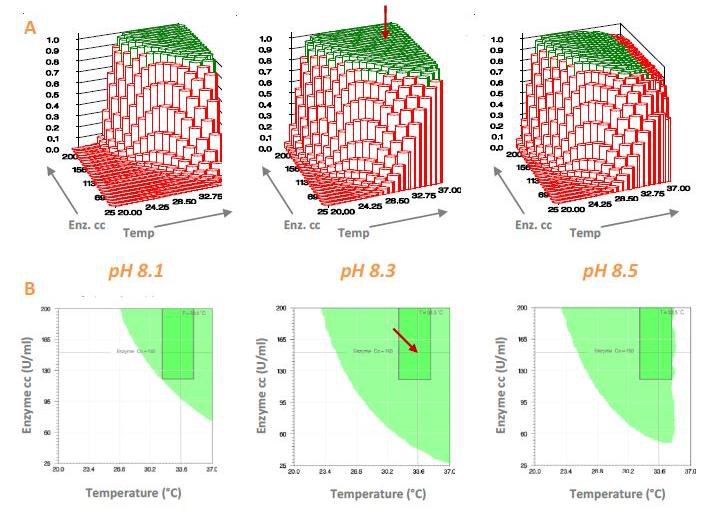
(A) Robustness surfaces showing the proportion of simulated results meeting the specifications as a function of temperature and enzyme concentration at pH 8.1, 8.3, and 8.5. (B) The Graphical design space, represented as green areas, is significantly larger than the tabulated design space (rectangles)
표
(A) Robustness surfaces showing the proportion of simulated results meeting the specifications as a function of temperature and enzyme concentration at pH 8.1, 8.3, and 8.5. (B) The Graphical design space, represented as green areas, is significantly larger than the tabulated design space (rectangles)
 표
(A) Robustness surfaces showing the proportion of simulated results meeting the specifications as a function of temperature and enzyme concentration at pH 8.1, 8.3, and 8.5. (B) The Graphical design space, represented as green areas, is significantly larger than the tabulated design space (rectangles)
표
(A) Robustness surfaces showing the proportion of simulated results meeting the specifications as a function of temperature and enzyme concentration at pH 8.1, 8.3, and 8.5. (B) The Graphical design space, represented as green areas, is significantly larger than the tabulated design space (rectangles)
| 과제명(ProjectTitle) : | - |
|---|---|
| 연구책임자(Manager) : | - |
| 과제기간(DetailSeriesProject) : | - |
| 총연구비 (DetailSeriesProject) : | - |
| 키워드(keyword) : | - |
| 과제수행기간(LeadAgency) : | - |
| 연구목표(Goal) : | - |
| 연구내용(Abstract) : | - |
| 기대효과(Effect) : | - |
Copyright KISTI. All Rights Reserved.

※ AI-Helper는 부적절한 답변을 할 수 있습니다.